I. 서 론
현대사회에서 골다공증(osteoporosis)은 높은 유병률과 이로부터 발생되는 골절 사망률 및 골다공증 관련 질병 치료비용의 증가로 인해 큰 사회적 문제로 대두되고 있다. 골다공증은 골대사의 이상으로 골 형성의 감소 및 골 흡수의 증가로 인해 골량의 감소를 일으켜 약한 충격에도 쉽게 골절을 발생시키는 전신적인 골질환으로 정의되며,[1] 최근 미국 국립보건원은 골강도(bone strength)의 약화로 인해 골절의 위험성이 증가하는 골격계 질환으로 규정하였다.[2] 골강도는 골밀도에 의해 표현되는 골량과 더불어 골미세구조, 골교체율, 무기질화 등으로 표현되는 골질에 의해 결정된다. 현재 임상에서는 골다공증 진단을 위해 단위면적당 또는 단위부피당 골밀도(bone mineral density)를 주로 측정하고 있다. 골밀도는 골다공증 진단을 위해 가장 유용한 지표로 알려져 있으며, 치료방침의 결정 및 뼈의 소실과 증가 속도 또는 치료에 대한 반응을 평가하는 용도로 이용된다.
인체의 뼈는 30% 이하의 다공율과 치밀한 구조를 갖는 피질골(cortical bone) 및 30% 이상의 다공율과 골소주(trabeculae)의 복잡한 그물 구조를 갖는 해면질골(trabecular bone)로 구성된다. 피질골은 골격을 이루는 뼈의 대부분에 이르는 80%의 골량을 차지한다. 그러나 부피에 대한 표면적은 해면질골이 피질골의 10배에 달하며, 피질골에 비해 대사자극에 8배 이상 빨리 반응한다고 알려져 있다. 이는 대사성 골질환인 골다공증에서 해면질골이 피질골에 비해 더 많은 영향을 준다는 것을 의미한다. 또한 골절로 인한 유병률 및 사망률이 높은 대퇴골 경부(femoral neck) 및 요추골(lumbar spine)은 해면질골이 밀집되어 있으므로 이들 부위의 골밀도 측정이 권장되고 있다.[3] 골다공증에 의한 대퇴골 골절환자 대부분에서 활동성에 제약이 발생되며, 60세 이상 노인인구에서 골반골절로 인한 30일 사망률은 9.6%, 1년 사망률은 33%로 매우 높게 나타나고 있다. 사망하지 않더라도 지속적인 장애를 야기할 수 있으며, 대퇴골 골절은 가장 심각한 병적상태로서 50%까지는 보조기구의 도움 없이 걷지 못하고, 33%까지는 독립적인 생활이 불가능해 이에 대한 예방이 필수적이다.[4]
골밀도 측정방법 중에 이중에너지 X-선 흡수계측법(Dual Energy X-ray Absorptiometry; DEXA)이 임상에서 가장 일반적으로 이용되는 방법이다. DEXA 장비는 골절 발생 시 사망률이 높은 대퇴골 경부 및 요추골을 측정부위로 하므로 골절의 위험도를 예측하기 위한 가장 이상적인 방법으로 알려져 있다. 그러나 치료반응을 감시하기 위한 반복적인 측정을 위해서는 방사선 노출의 부담이 필연적으로 존재한다. 현재 골다공증 진단을 위해 임상에서 이용되고 있는 정량적 초음파(Quantitative UltraSound; QUS) 기술은 말초 골격계의 골밀도를 평가할 수 있는 방법으로서 측정부위로 종골(calcaneus)이라 불리는 발뒤꿈치뼈에서 음속(Speed Of Sound; SOS) 및 광대역 초음파 감쇠(normalized Broadband Ultrasound Attenuation; nBUA)를 측정한다. 종골은 양쪽 면이 서로 평행하여 초음파가 투과하기에 용이하고, 양쪽 면 사이에 해면질골을 많이 포함하고 있으며, 해면질골의 음향특성에 영향을 미칠 수 있는 피질골의 두께가 매우 얇은 장점을 갖고 있다. 골다공증은 골대사의 이상으로 발생되는 전신적인 골질환이므로 종골의 골밀도는 골절 위험도가 높은 대퇴골 경부 및 요추골의 골밀도와 높은 상관관계를 갖는 것으로 알려져 있다.[5] QUS는 DEXA에 비해 골밀도 측정의 정확도가 상대적으로 낮아 정확도의 개선이 요구되고 있지만, X-선을 이용하지 않으므로 방사선의 노출이 전혀 없어 골다공증 중증환자에게 반복적인 검사가 가능할 뿐만 아니라 진단기기의 가격 및 진단비용이 상대적으로 저렴하여 DEXA보다 쉽게 널리 이용될 수 있는 장점을 갖고 있다.[6]
종골과 같은 말초 골격계 해면질골의 외부껍질을 구성하는 피질골은 높은 밀도 및 치밀한 구조로 인해 해면질골의 음향특성에 상당한 효과를 미치는 것으로 알려져 있다. Xia 등은 생체 외 조건의 종골에서 측정된 nBUA가 해면질골의 양보다 피질골의 두께에 더 큰 영향을 받는다고 보고하였으며,[7] 여러 연구자들이 생체 외 조건의 종골에서 피질골의 제거 전후에 나타나는 nBUA 및 SOS의 변화를 보고하였다.[8, 9] 종골에서 해면질골을 둘러싸는 피질골이 해면질골의 음향특성에 미치는 효과가 다수 보고된 것과 달리 골절 위험도가 높은 대퇴골에서 종골에 비해 상대적으로 더 두꺼운 두께를 갖는 대퇴골의 피질골이 해면질골의 음향특성에 미치는 효과는 보고되지 않은 실정이다. 본 연구에서는 생체 외 조건의 소 대퇴골에서 피질골이 해면질골의 SOS 및 nBUA와 같은 음향특성에 미치는 효과를 조사하기 위해 2개의 소 대퇴골을 이용하여 근위부로부터 12개의 해면질골 샘플 및 서로 다른 두께를 갖는 3개의 피질골 판을 제작하였다. 또한 해면질골 샘플에 피질골 판 부착 전후 측정된 음향특성과 해면질골 겉보기 골밀도 사이의 상관관계를 조사하였다.
II. 대상 및 방법
2.1. 샘플 제작
본 연구에서는 2개의 소 대퇴골을 이용하여 근위부로부터 충분히 넓은 범위의 골밀도를 갖는 12개의 해면질골 샘플 및 서로 다른 두께를 갖는 3개의 피질골 판을 제작하였다. 12개의 해면질골 샘플은 전기톱을 이용하여 피질골이 완전히 제거되어 양쪽 면이 평행한 육면체의 형태로 제작하였으며, 14.5 ± 1.8 mm(평균값 ± 표준편차)의 두께를 가졌다. 3개의 피질골 판은 각각 1.00, 1.47, 및 2.00 mm의 두께를 갖는 얇은 판의 형태로 제작하였다. 또한 모든 해면질골 샘플 및 피질골 판은 본 연구에서 이용된 초음파 트랜스듀서의 중심 로브의 폭인 15 mm보다 큰 폭을 갖도록 제작하였다. 해면질골 샘플 내부의 골수는 음향특성 측정 전에 100°C 이상의 수중에서 가열하여 제거하였으며, 약 1 mmHg의 압력의 진공 데시케이터에서 약 8시간 동안 보관하여 샘플 내부의 기포를 모두 제거하였다. Fig. 1은 본 연구에서 이용된 1개의 대표적인 해면질골 샘플 및 서로 다른 두께를 갖는 3개의 피질골 판을 촬영한 사진을 나타낸다.
|
Fig. 1. Photograph of a typical trabecular bone sample and three cortical bone plates with different thickness used in the present study. |
2.2. SOS 및 nBUA 측정
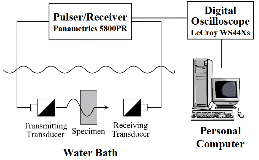
해면질골 샘플의 SOS 및 nBUA는 Fig. 2에 나타낸 실험장치 개략도와 같이 22°C의 온도를 갖는 수중에서 투과법을 이용하여 측정하였다.[10] 본 연구에서 이용된 25.4 mm의 직경 및 0.5 MHz의 중심주파수를 갖는 한 쌍의 광대역 비집속형 트랜스듀서(V301, Panametrics, Waltham, MA, USA)는 근거리 음장 길이(54 mm)의 두 배가 되는 거리에 서로 마주 보도록 설치하였다. 초음파 펄스를 송신 및 수신하기 위해 펄서/리시버(5800PR, Panametrics, Waltham, MA, USA)를 이용하였으며, 수신된 초음파 신호를 관찰 및 수집하기 위해 디지털 오실로스코프(WS44Xs, LeCroy, Chestnut Ridge, NY, USA)를 이용하였다. 해면질골 샘플은 그 중심이 초음파의 빔폭이 가장 작아지는 초음파 트랜스듀서의 근거리 음장 길이와 일치하는 지점에 설치하였다. 본 연구에서는 피질골 판이 부착되지 않은 해면질골 샘플(CTh.0)과 초음파가 수직으로 입사되는 샘플의 한쪽 면에 얇은 고무줄을 이용하여 각각 1.00(CTh.1.00), 1.47(CTh.1.47), 및 2.00 mm (CTh.2.00)의 두께를 갖는 피질골 판이 부착된 해면질골 샘플에 대해 SOS 및 nBUA를 측정하였다. 음향특성은 샘플의 중심으로부터 위치를 변화시켜가며 서로 다른 10개의 관심영역에 대해 측정하였다.
|
Fig. 2. Schematic diagram of the experimental setup for the measurements of SOS and nBUA of trabecular bone samples by using a through-transmission method in water. |
해면질골 샘플의 SOS 및 nBUA는 근거리 음장 길이의 두 배가 되는 거리(2 × 54 mm = 108 mm)에 서로 마주 보도록 설치된 초음파 트랜스듀서 사이에 샘플이 없는 경우 및 있는 경우에 수신된 초음파 신호를 이용하여 측정하였다. SOS(m/s)는 다음의 식(1)을 이용하여 계산하였다.[10]
| (1) |
여기서 ![]() 는 수중에서의 음속(1489 m/s @ 22°C),
는 수중에서의 음속(1489 m/s @ 22°C), ![]() 는(피질골 판의 두께를 포함하는) 샘플의 두께, 및
는(피질골 판의 두께를 포함하는) 샘플의 두께, 및 ![]() (
(![]() )는 초음파 트랜스듀서 사이에 샘플이 없는 경우에 수신된 초음파 신호의 수신시간(
)는 초음파 트랜스듀서 사이에 샘플이 없는 경우에 수신된 초음파 신호의 수신시간(![]() )과 샘플이 있는 경우에 수신된 초음파 신호의 수신시간(
)과 샘플이 있는 경우에 수신된 초음파 신호의 수신시간(![]() )의 차이를 나타낸다. nBUA를 결정하기 위해 먼저 아래의 식(2)를 이용하여 샘플의 감쇠계수
)의 차이를 나타낸다. nBUA를 결정하기 위해 먼저 아래의 식(2)를 이용하여 샘플의 감쇠계수 ![]() (dB/cm)를 계산하였다.[10]
(dB/cm)를 계산하였다.[10]
| (2) |
여기서 ![]() 및
및 ![]() 는 초음파 트랜스듀서 사이에 샘플이 없는 경우 및 있는 경우에 수신된 초음파 신호의 파워스펙트럼레벨 및
는 초음파 트랜스듀서 사이에 샘플이 없는 경우 및 있는 경우에 수신된 초음파 신호의 파워스펙트럼레벨 및 ![]() 는(피질골 판의 두께를 포함하는) 샘플의 두께를 나타낸다. 특성감쇠계수라고도 불리는 샘플의 nBUA(dB/cm/MHz)는 특정 주파수 범위에서 주파수에 대해 선형적으로 증가하는
는(피질골 판의 두께를 포함하는) 샘플의 두께를 나타낸다. 특성감쇠계수라고도 불리는 샘플의 nBUA(dB/cm/MHz)는 특정 주파수 범위에서 주파수에 대해 선형적으로 증가하는 ![]() 의 기울기로부터 결정하였다.
의 기울기로부터 결정하였다.
III. 결과 및 고찰
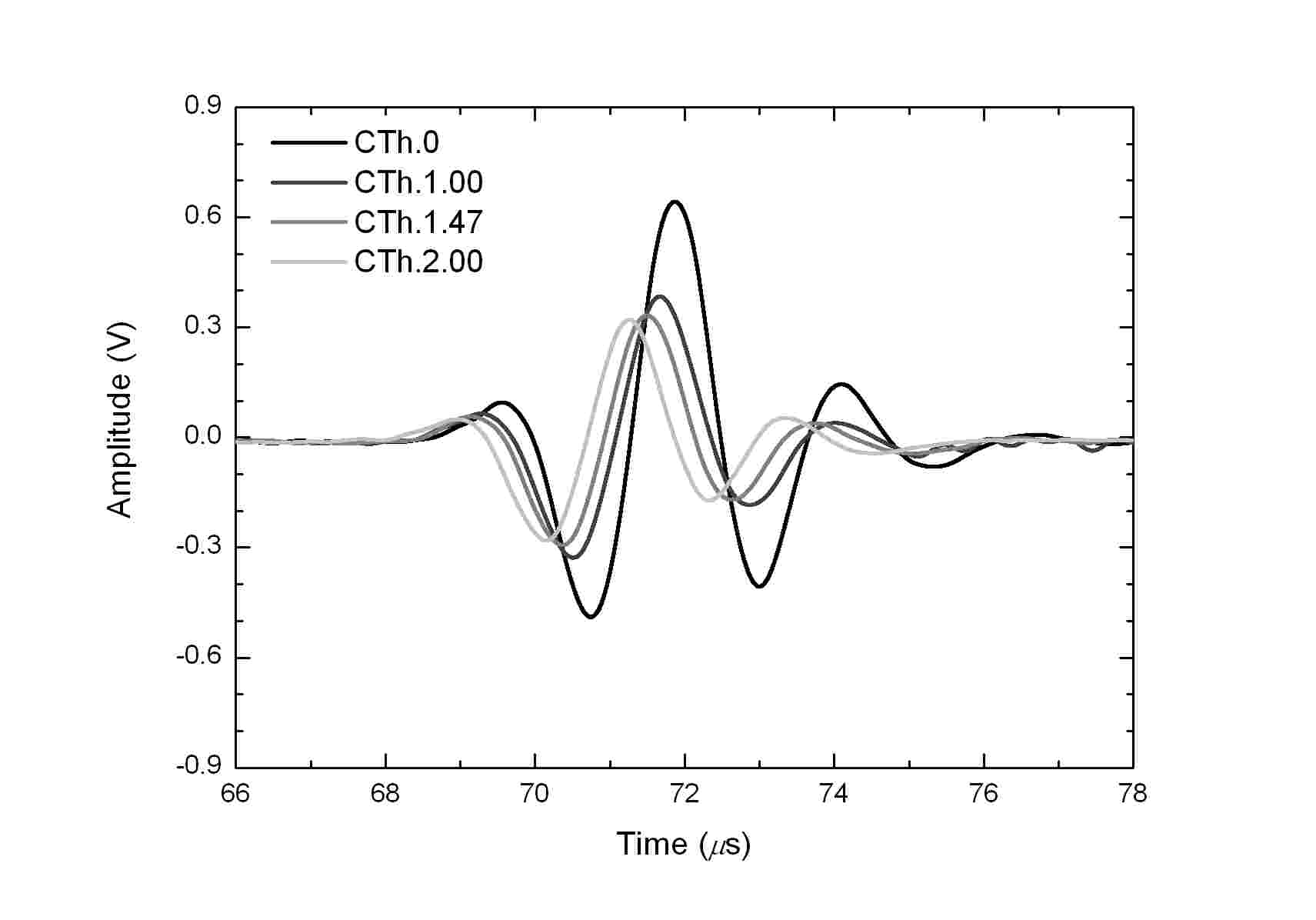
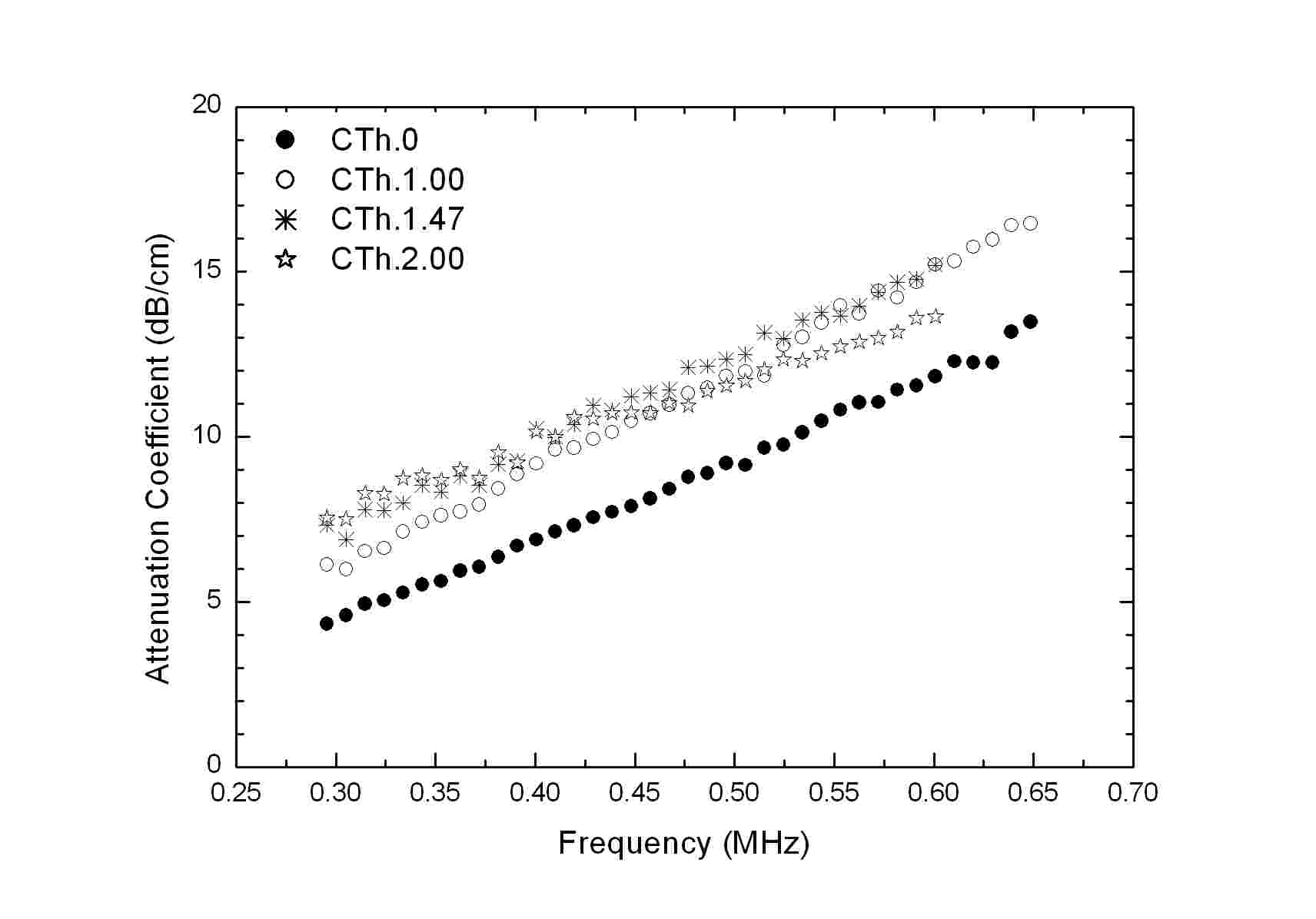
Fig. 3은 1개의 대표적인 해면질골 샘플의 한쪽 면에 피질골 판이 부착되지 않은 경우 및 부착된 경우에 수신된 초음파 신호를 나타낸다. CTh.0는 피질골 판이 부착되지 않은 해면질골 샘플을 나타내며, CTh.1.00, CTh.1.47, 및 CTh.2.00는 초음파가 수직으로 입사되는 샘플의 한쪽 면에 각각 1.00, 1.47, 및 2.00 mm의 두께를 갖는 피질골 판이 부착된 해면질골 샘플을 나타낸다. Fig. 3에서 볼 수 있듯이 해면질골에 비해 높은 밀도 및 음속을 갖는 피질골 판의 두께가 증가함에 따라 더욱 빠른 수신시간을 보였으며, 수신진폭은 감소하는 것으로 나타났다. Fig. 4는 CTh.0, CTh.1.00, CTh.1.47, 및 CTh.2.00에 대해 측정된 감쇠계수를 주파수 함수로 나타낸 것이다. Fig. 4에서 볼 수 있듯이 서로 다른 두께를 갖는 피질골 판의 영향으로 인해 감쇠계수가 서로 다른 특정 주파수 범위에서 주파수에 대해 선형적으로 증가하는 것을 알 수 있다. CTh.0 및 CTh.1.00은 0.3 - 0.65 MHz의 주파수 범위에서 nBUA를 결정하였으며, CTh.1.47 및 CTh. 2.00은 0.3 - 0.6 MHz의 주파수 범위에서 nBUA를 결정하였다.
Table 1은 피질골 판이 부착되지 않은 해면질골 샘플(CTh.0) 및 초음파가 수직으로 입사되는 샘플의 한쪽 면에 각각 1.00(CTh.1.00), 1.47(CTh.1.47), 및 2.00 mm (CTh.2.00)의 두께를 갖는 피질골 판이 부착된 해면질골 샘플에 대해 측정된 해면질골 겉보기 골밀도, SOS, 및 nBUA의 평균값 및 표준편차를 나타낸다. Table 1에서 볼 수 있듯이 겉보기 골밀도 측정법을 이용하여 측정된 피질골 판이 부착되지 않은 12개 CTh.0의 겉보기 골밀도는 0.362 - 0.633 g/cm3의 범위에 분포하였으며, 0.474 ± 0.086 g/cm3의 평균값을 가졌다. 본 연구에서 이용된 12개의 해면질골 샘플에서 측정된 겉보기 골밀도의 평균값은 14개의 사람 대퇴골을 이용하여 제작된 23개의 해면질골 샘플에서 측정된 겉보기 골밀도의 평균값(0.483 ± 0.162 g/cm3)과 매우 유사한 것으로 나타났다.[11] CTh.0의 SOS는 1706 ± 119 m/s의 평균값을 가졌으며, 피질골 판이 부착된 CTh.1.00, CTh.1.47, 및 CTh.2.00의 SOS는 CTh.0의 SOS에 비해 17, 53, 및 68 m/s만큼 거의 선형적으로 증가하였다. 또한 Table 1에서 볼 수 있듯이 CTh.0의 nBUA는 22.2 - 48.9 dB/cm/MHz의 범위에 분포하였으며, 33.2 ± 10.3 dB/cm/MHz의 평균값을 가졌다. 반면에 CTh.1.00의 nBUA는 34.9 ± 7.6 dB/cm/MHz의 값을 가졌으며, CTh.1.47 및 CTh.2.00의 nBUA는 각각 CTh.0 및 CTh.1.00의 nBUA보다 작은 30.1 ± 9.3 및 23.9±8.9 dB/cm/MHz의 값을 갖는 것으로 나타났다. 즉 피질골 판의 두께가 증가함에 따라 거의 선형적으로 증가하는 SOS에 비해 nBUA는 피질골 판의 두께에 대해 비선형적인 의존성을 나타내는 것을 알 수 있다.
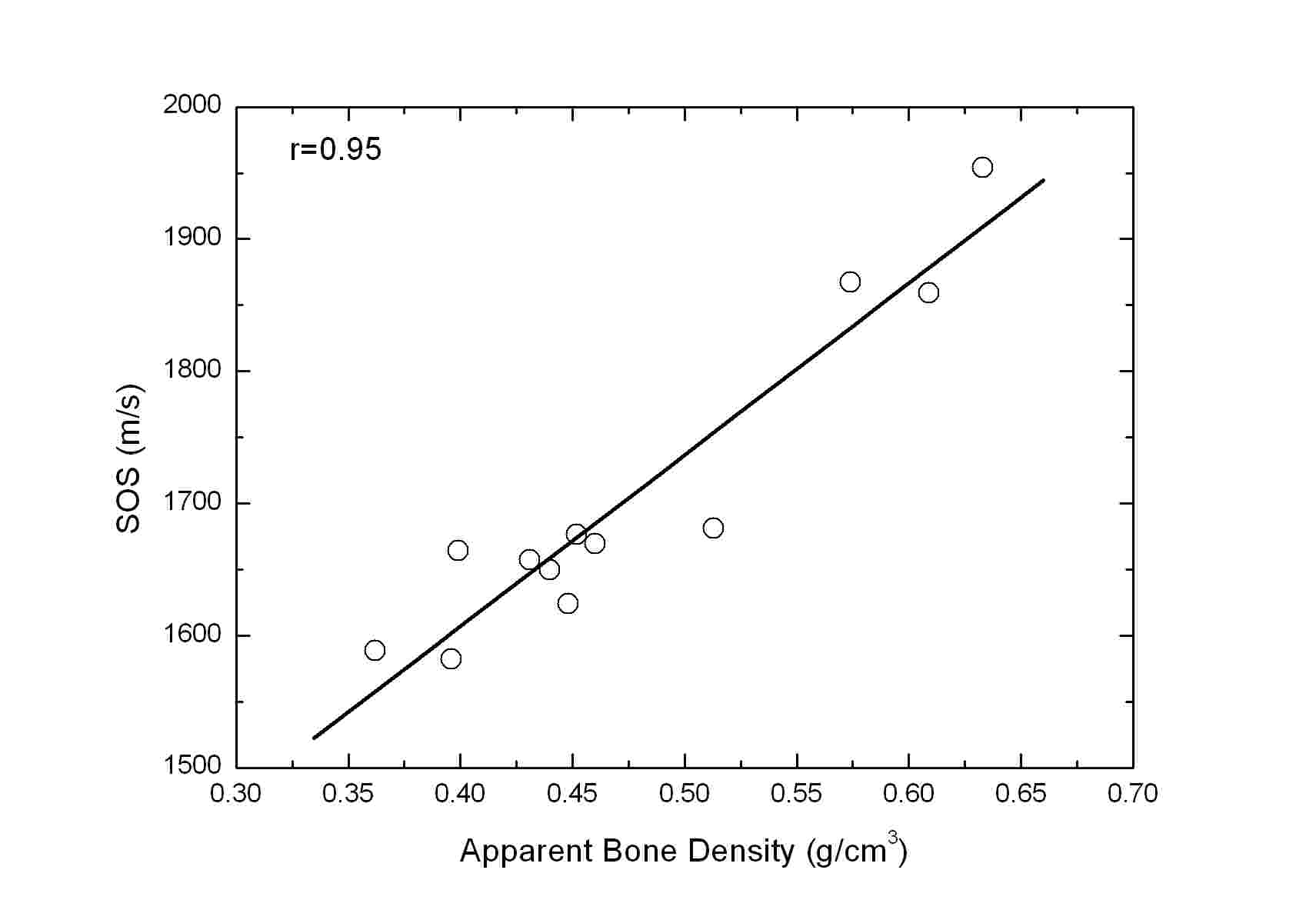
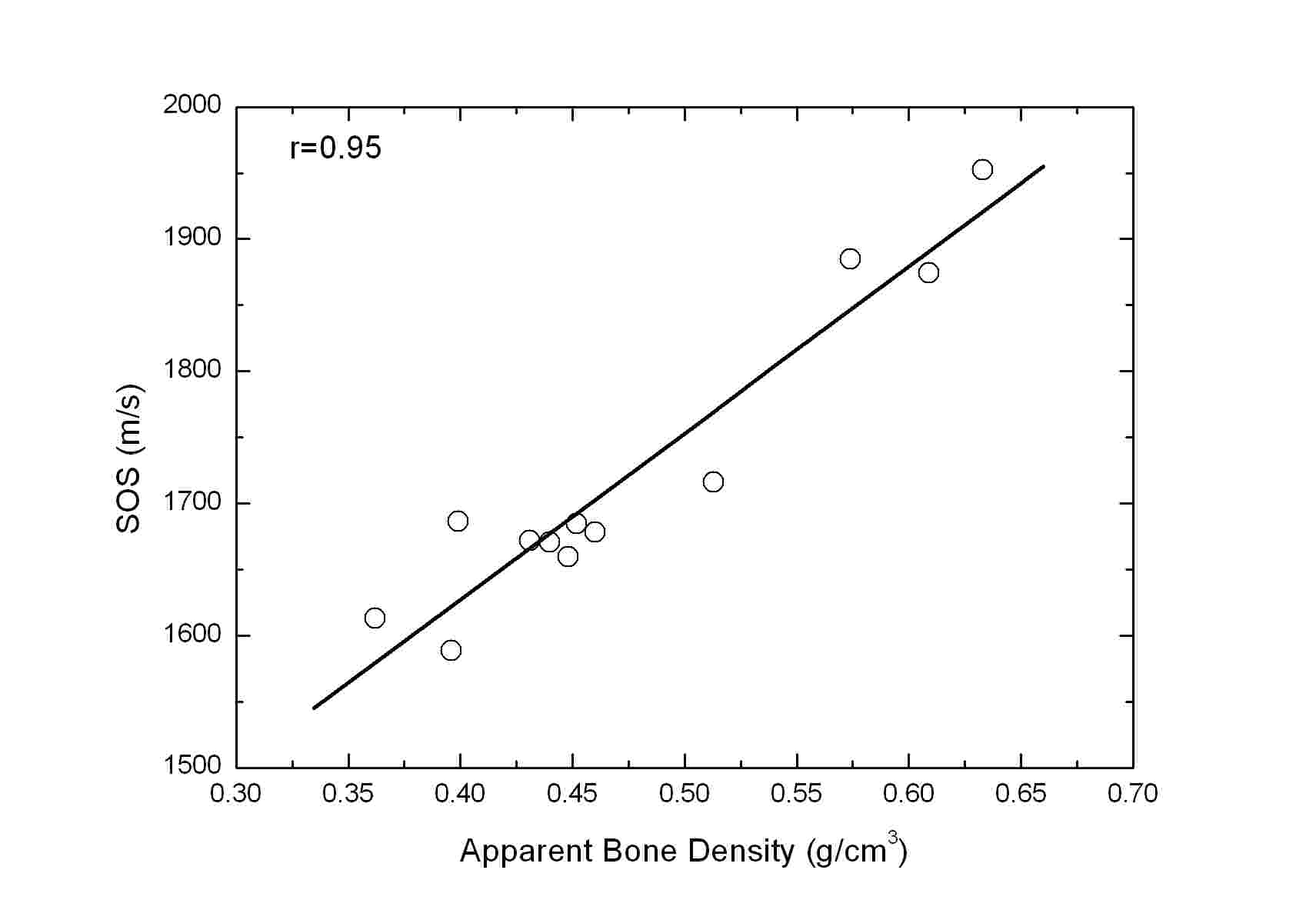
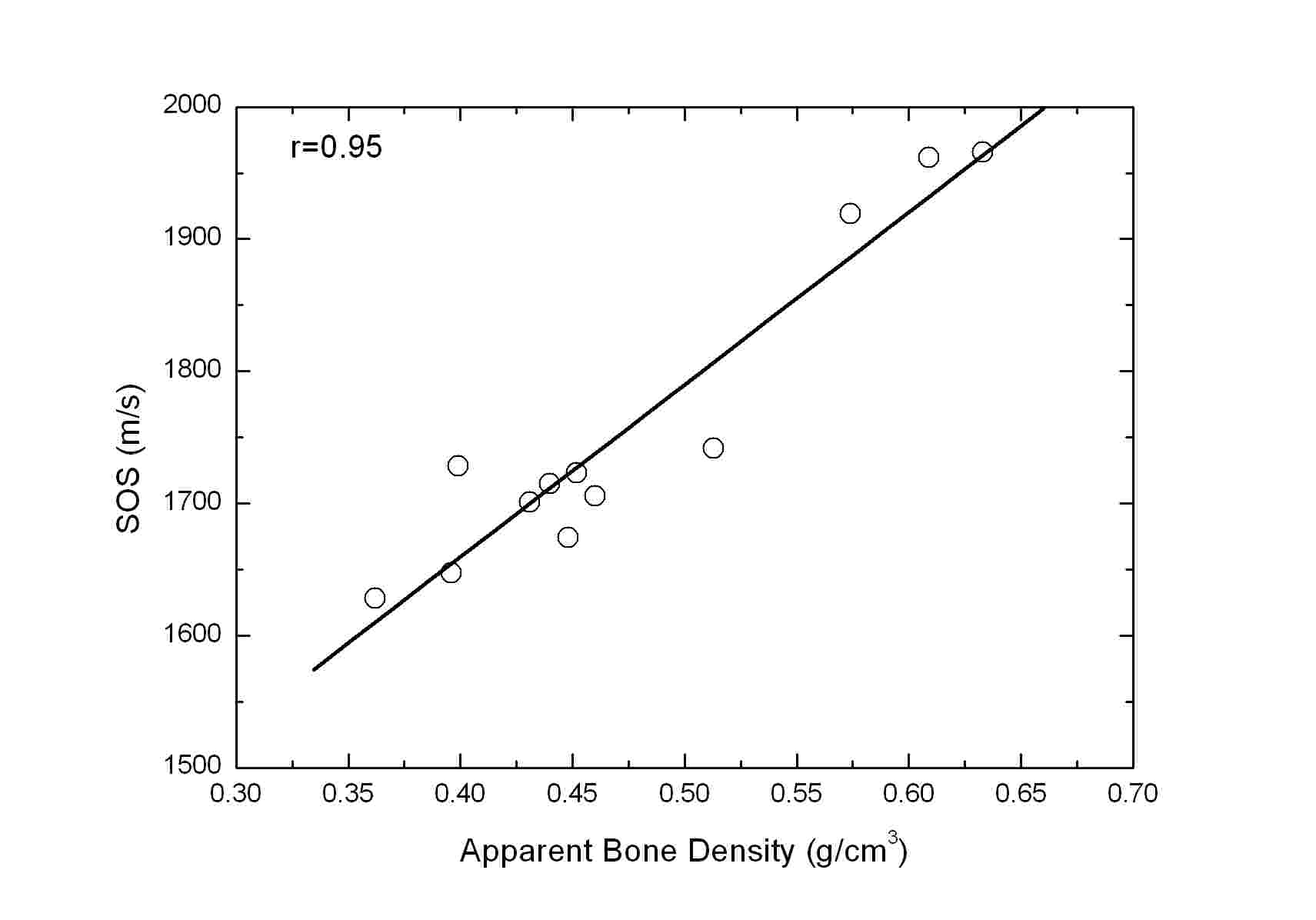
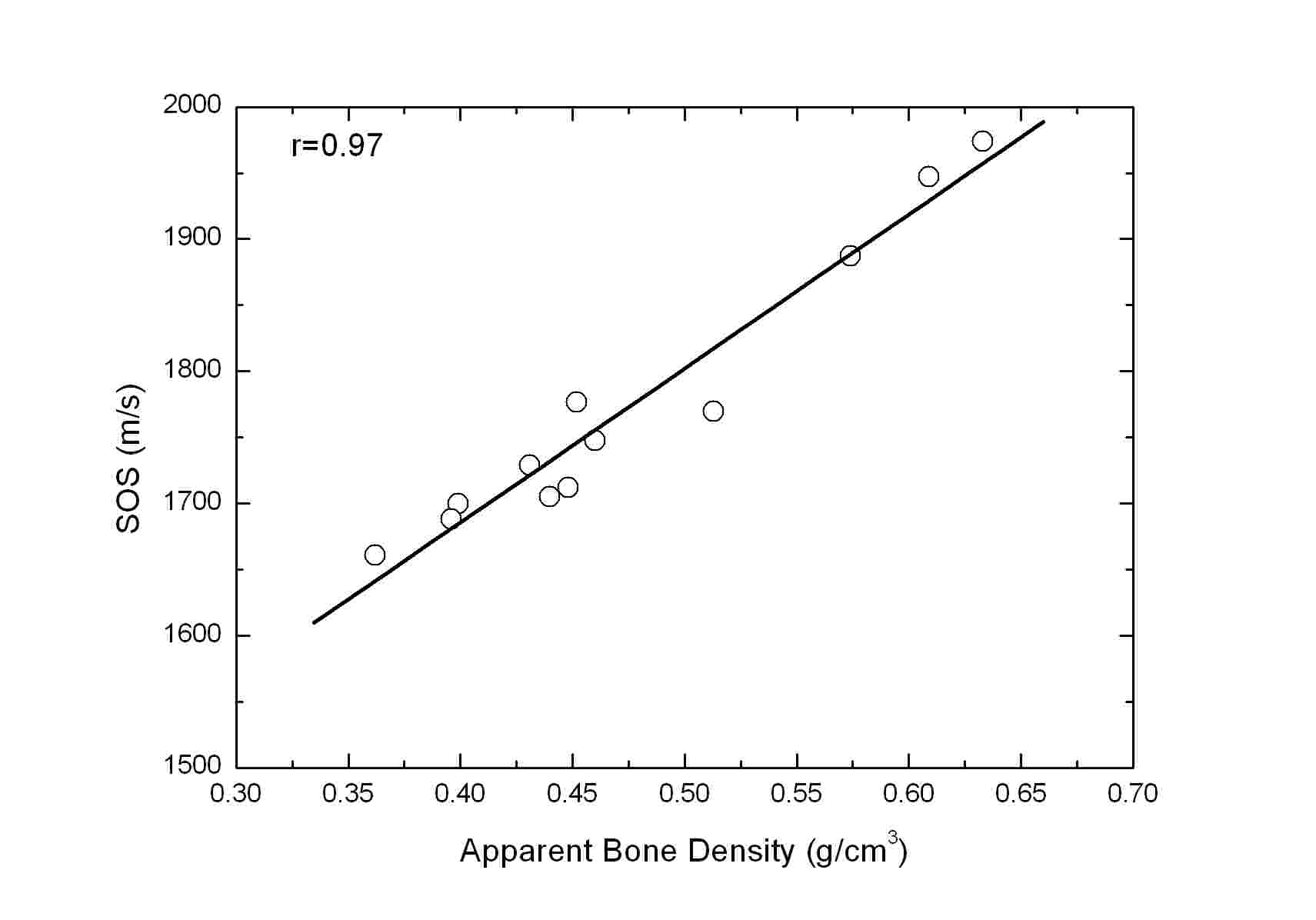
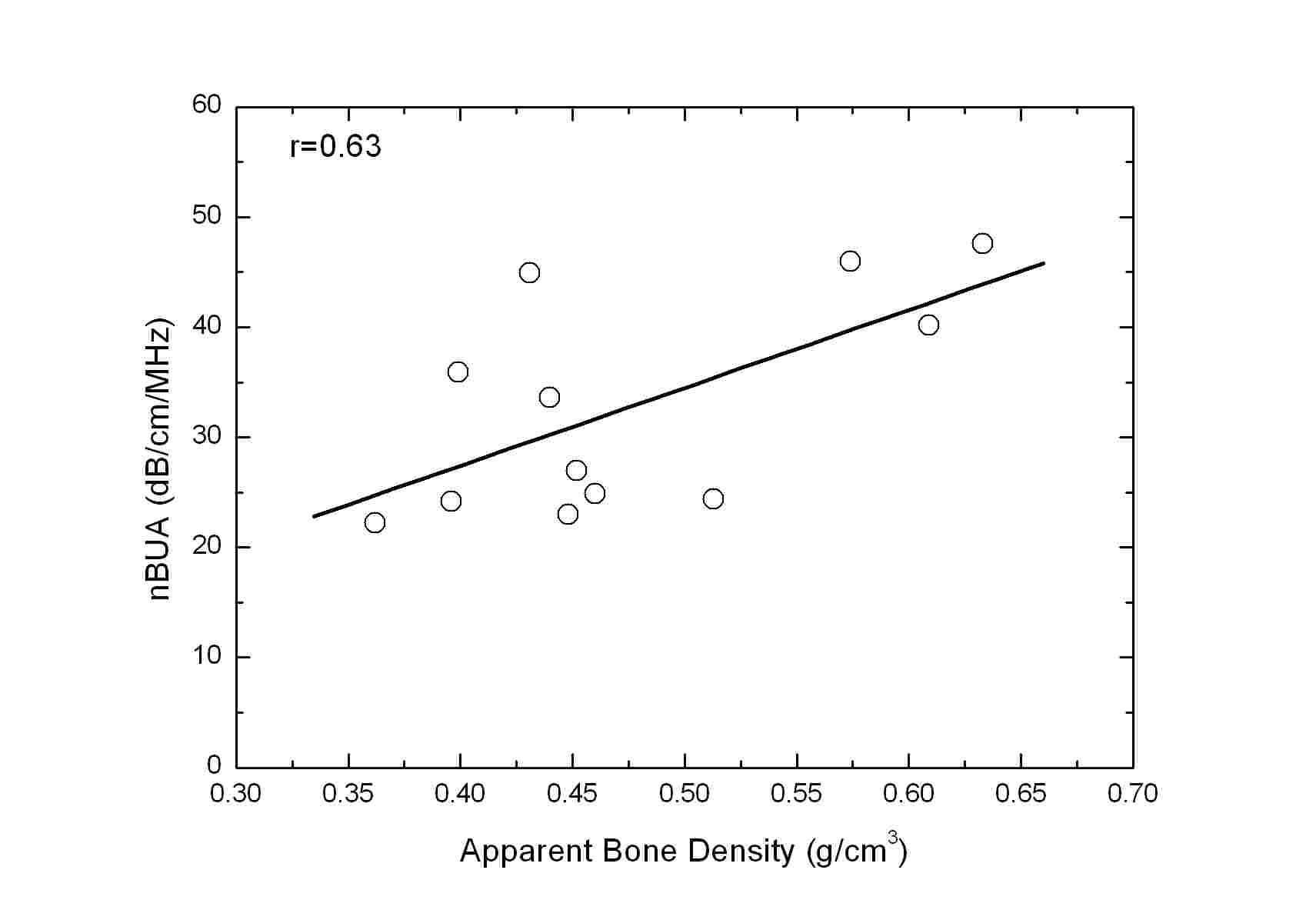
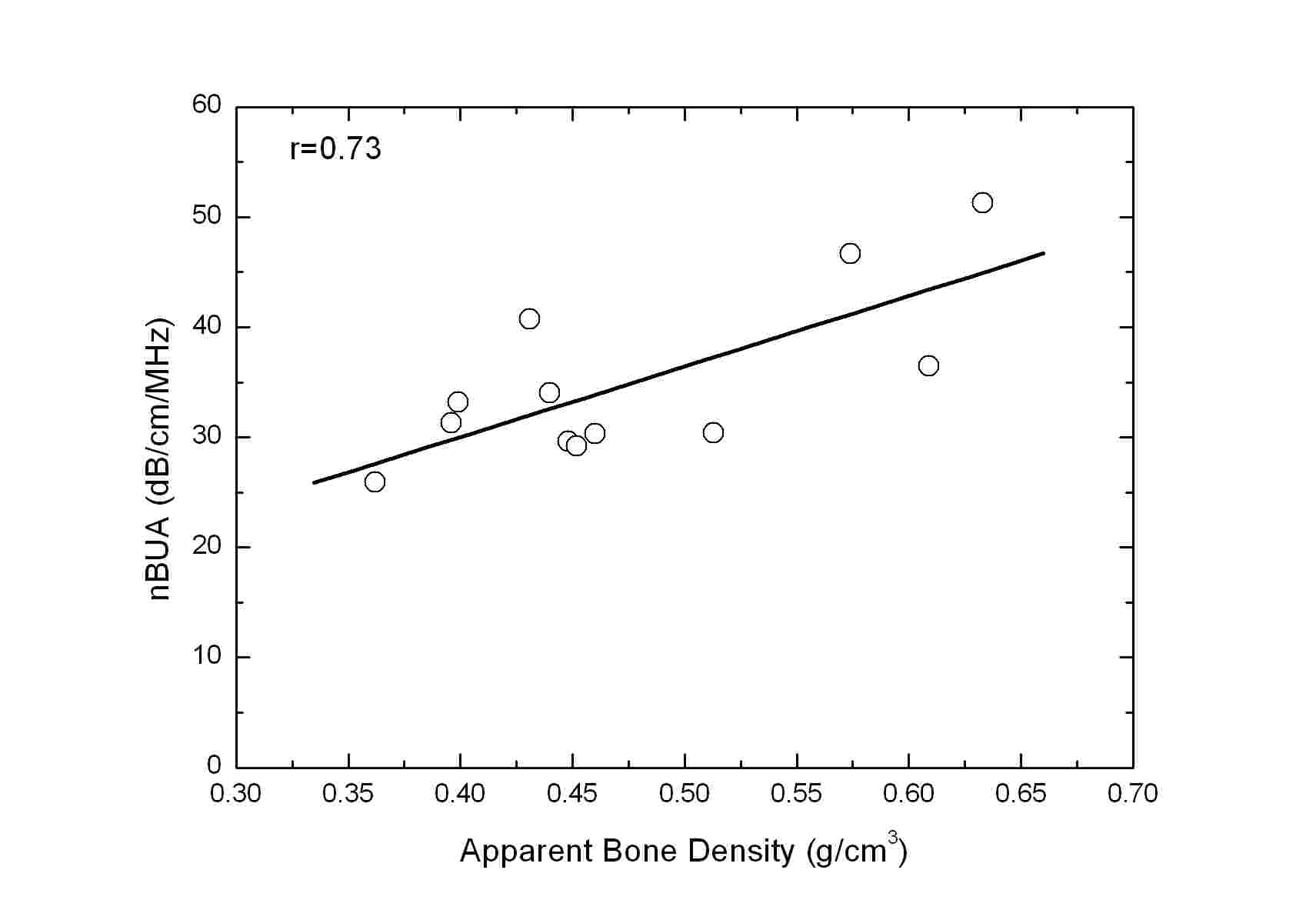
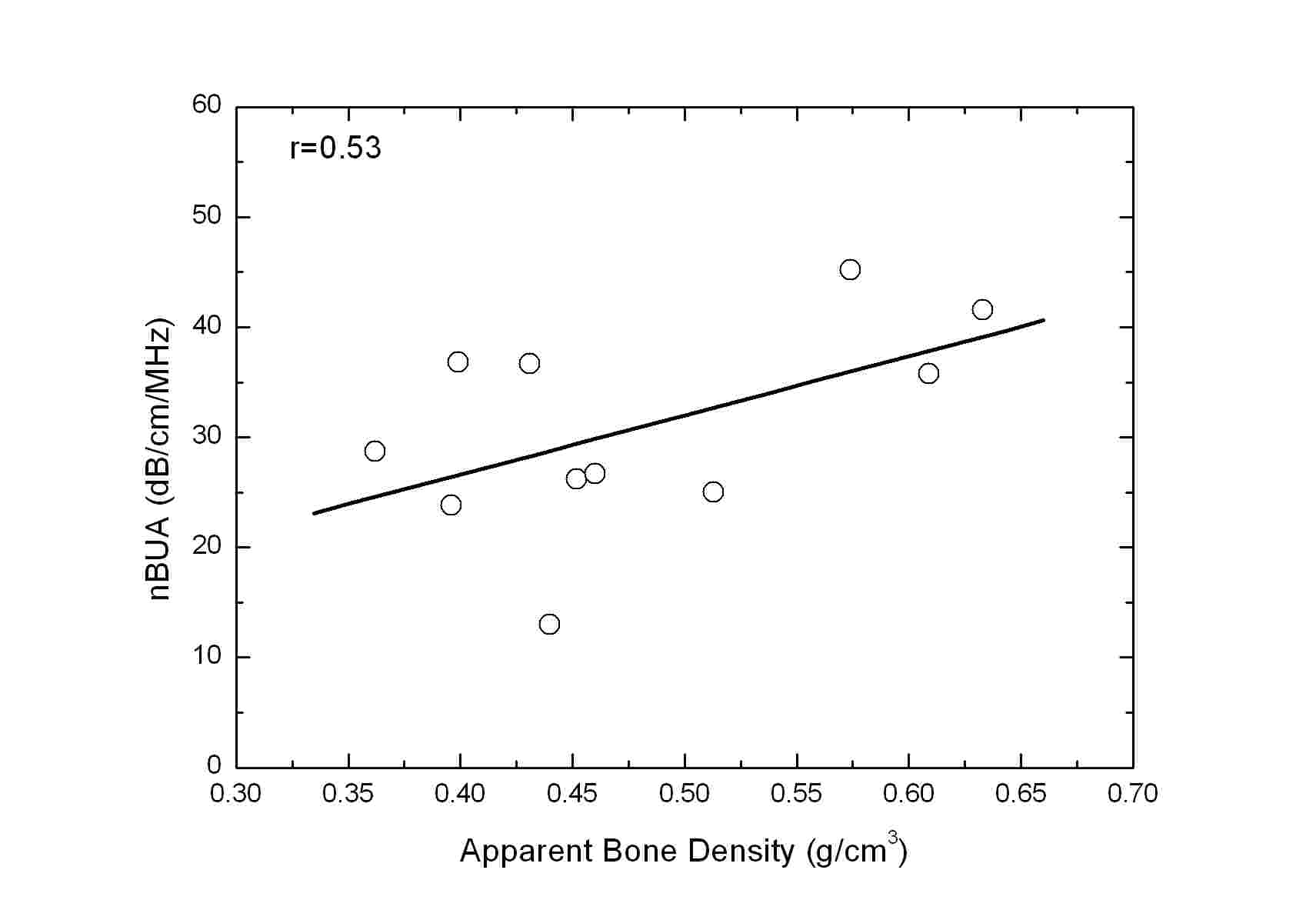
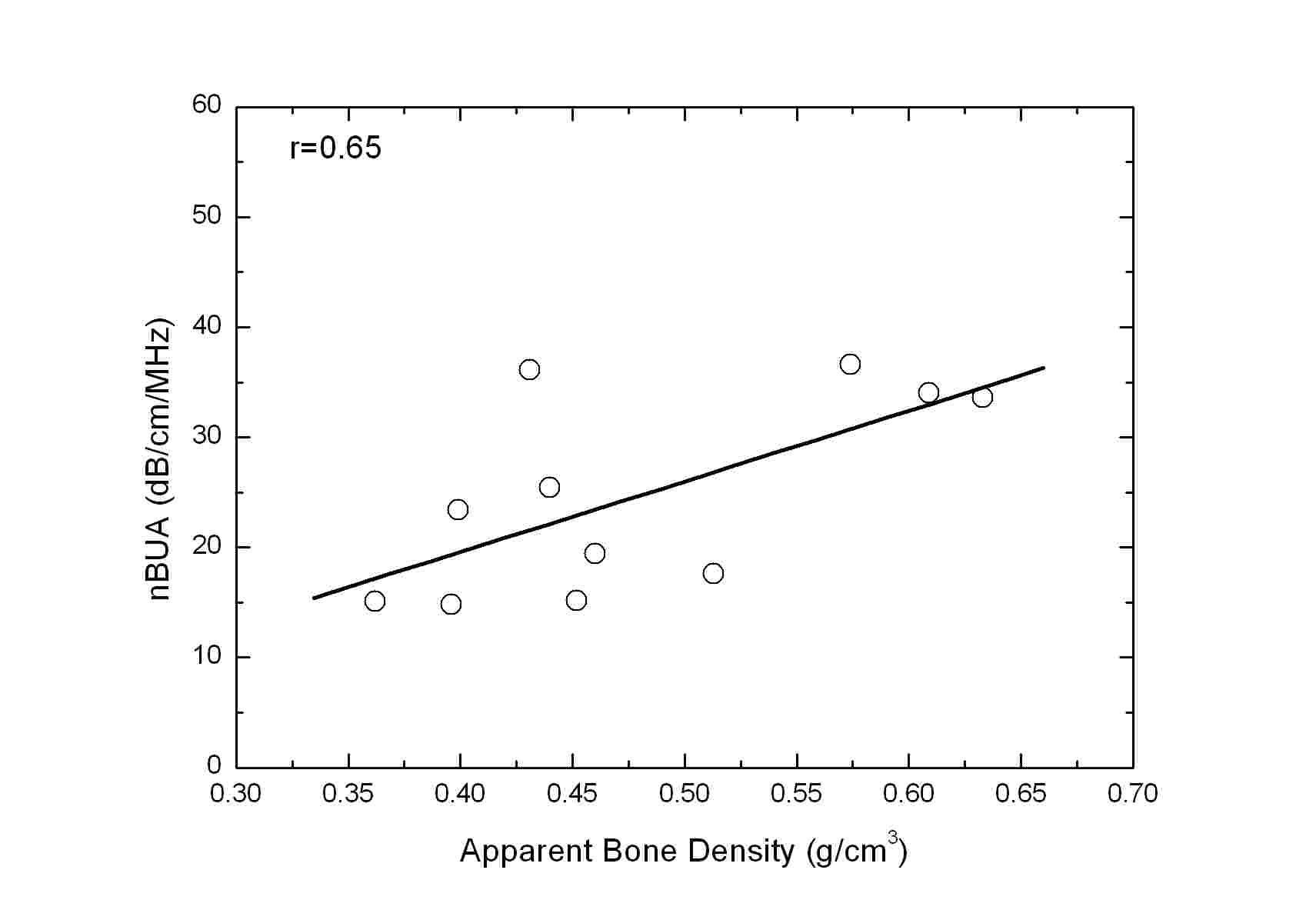
Table 2는 CTh.0, CTh.1.00, CTh.1.47, 및 CTh.2.00에 대해 측정된 해면질골 겉보기 골밀도 및 SOS 사이의 Pearson 상관계수(r)를 나타낸다(모든 r에 대해 p < 0.0001). Table 2에서 볼 수 있듯이 해면질골 겉보기 골밀도와 SOS 사이의 r은 0.9 5 - 0.97의 매우 높은 값을 갖는 것으로 나타났다. 여기서 주목할 점은 초음파가 수직으로 입사되는 샘플의 한쪽 면에 서로 다른 두께를 갖는 피질골 판이 부착된 CTh.1.00, CTh.1.47, 및 CTh.2.00의 SOS의 경우에도 해면질골 겉보기 골밀도와 강한 상관관계를 나타낸다는 것이다. 또한 CTh.0, CTh.1.00, CTh.1.47, 및 CTh.2.00의 SOS 사이에도 r = 0.97 - 0.99의 매우 높은 상관관계가 존재하는 것으로 나타났다. 반면에 Table 3에 나타낸 CTh.0, CTh. 1.00, CTh.1.47, 및 CTh.2.00에 대해 측정된 해면질골 겉보기 골밀도 및 nBUA 사이에는 r = 0.53 - 0.73의 상관관계를 갖는 것으로 나타났다. CTh.0, CTh.1.00, CTh.1.47, 및 CTh.2.00의 nBUA 사이에는 r = 0.67 - 0.96의 비교적 강한 상관관계가 존재하는 것으로 나타났다. Fig. 5 및 6은 CTh.0, CTh.1.00, CTh.1.47, 및 CTh. 2.00에 대해 측정된 SOS 및 nBUA를 해면질골 겉보기 골밀도 함수로 나타낸 것이다. 그림의 ○ 기호는 각각의 해면질골 샘플에 대해 샘플의 중심으로부터 위치를 변화시켜가며 서로 다른 10개의 관심영역에 대해 측정된 SOS 및 nBUA의 평균값을 나타내며, 흑색 실선으로 나타낸 직선은 이들 평균값에 대한 선형회귀(linear regression)를 나타낸다.
본 연구에서 이용된 12개의 소 대퇴골 해면질골 샘플에서 측정된 SOS는 1582-1954 m/s로서 Padilla 등에 의해 보고된 사람의 대퇴골 해면질골 샘플에서 측정된 SOS(1485 - 1812 m/s)와 유사한 값을 갖는 것으로 나타났다.[12] 또한 소의 대퇴골로부터 제작된 피질골 샘플에서 측정된 SOS는 2200 - 2450 m/s로서 사람의 피질골에서 측정된 SOS(2500 - 3600 m/s) 보다 다소 작은 값을 갖는 것으로 나타났다.[13, 14] 이와 같이 높은 밀도 및 치밀한 구조를 갖는 피질골은 낮은 밀도 및 높은 다공율을 갖는 해면질골에 비해 더 큰 SOS를 가지며, 해면질골 샘플의 초음파 입사면에 부착된 피질골 판의 두께 증가는 SOS 증가의 원인이 된다. 즉 Table 1에서 볼 수 있듯이 피질골 판이 부착된 CTh.1.00, CTh.1.47, 및 CTh.2.00의 SOS는 CTh.0의 SOS에 비해 17, 53, 및 68 m/s만큼 증가하는 것으로 나타났다. 그러나 Table 2에서 볼 수 있듯이 서로 다른 두께를 갖는 피질골 판이 부착되더라도 SOS와 해면질골 겉보기 골밀도 사이의 높은 상관관계는 유지되는 것을 알 수 있다. 이와 같은 결과는 생체 외 조건에서 사람의 종골 샘플을 이용하여 피질골 판이 음속에 미치는 효과를 조사한 다른 연구자들에 의해 보고된 결과와 잘 일치한다. 예를 들면 Njeh 및 Langton은 골수를 제거하지 않은 20개의 원통형 종골 샘플에서 피질골 판을 제거한 후에 1.0 MHz의 중심주파수를 갖는 초음파 트랜스듀서를 이용하여 측정된 SOS가 38 m/s 만큼 감소하고, 피질골의 제거 전후 측정된 SOS와 해면질골 겉보기 골밀도 사이에 높은 상관관계(r = 0.69 - 0.85)가 나타나는 것을 관찰하였다.[9] 이들 선행연구를 비롯하여 본 연구의 결과로부터 SOS는 종골에 비해 상대적으로 더 두꺼운 피질골 두께를 갖는 대퇴골에서 측정되더라도 해면질골의 골밀도를 예측하기에 충분한 지표임을 알 수 있다. 향후에는 Njeh 및 Langton의 연구와 마찬가지로 생체 내 조건의 대퇴골과 더욱 유사한 상황을 위해 초음파가 수직으로 투과되는 해면질골 샘플의 양쪽 면에 피질골 판을 부착하여 측정된 SOS와 골밀도 사이의 상관관계를 조사할 필요가 있다.
골소주가 3차원의 그물 구조를 가지며, 90% 이상의 높은 다공율을 갖는 해면질골에서 초음파의 감쇠는 흡수 및 산란으로 인해 발생되며, 특정 주파수 범위에서 주파수에 대해 선형적으로 증가하는 것으로 나타난다.[15] 예를 들면 Lee 및 Choi는 생체 외 조건에서 소 대퇴골 해면질골 샘플을 이용하여 감쇠계수가 0.2-0.7 MHz의 주파수 범위에서 주파수 ![]() 에 대해
에 대해 ![]() 의 의존성을 나타내는 것을 보고하였다.[16] 생체 내 조건에서 해면질골을 둘러싸는 피질골의 두께가 1 mm 미만인 종골의 경우에도 연조직/해면질골 또는 물/해면질골 경계면에서 반사로 인해 발생되는 투과손실이 무시될 수 있을 정도로 매우 작으므로 감쇠계수의 주파수에 대한 선형적인 의존성이 보존되는 것으로 알려져 있다.[17] 반면에 본 연구에서처럼 해면질골 샘플의 초음파 입사면에 높은 밀도 및 음속을 갖는 피질골 판이 부착된 경우에는 정확한 감쇠계수를 구하기 위해 물/피질골 경계면에서 발생되는 투과손실이 보정되어야 한다. 그러므로 본 연구와 같이 식(2)로부터 얻어진 CTh.1.00, CTh.1.47, 및 CTh.2.00에 대한 감쇠계수는 임상에서 이용되는 초음파 골밀도 측정기의 경우와 마찬가지로 물/피질골 경계면에서 반사로 인해 발생되는 투과손실이 보정되지 않았으므로 엄밀히 말하면 겉보기 감쇠라고 할 수 있다. Fig. 4에서 볼 수 있듯이 서로 다른 두께를 갖는 피질골 판의 효과(피질골 경계면에서의 반사 및 피질골 내에서의 감쇠)로 인해 감쇠계수가 CTh.0 및 CTh.1.00의 경우에는 0.3-0.65 MHz, CTh.1.47 및 CTh.2.00의 경우에는 0.3-0.6 MHz와 같은 서로 다른 주파수 범위에서 선형적으로 증가하며, 또한 nBUA는 피질골 판의 두께에 대해 비선형적인 의존성을 나타내는 것을 알 수 있다. 본 연구와 유사하게 Xia 등도 18개의 사람 종골 샘플을 이용하여 해면질골 샘플의 양쪽 면에 존재하는 0.3 및 0.6 mm의 두께를 갖는 피질골 판이 nBUA의 측정에 큰 효과를 미치는 것을 보고하였다.[7]
의 의존성을 나타내는 것을 보고하였다.[16] 생체 내 조건에서 해면질골을 둘러싸는 피질골의 두께가 1 mm 미만인 종골의 경우에도 연조직/해면질골 또는 물/해면질골 경계면에서 반사로 인해 발생되는 투과손실이 무시될 수 있을 정도로 매우 작으므로 감쇠계수의 주파수에 대한 선형적인 의존성이 보존되는 것으로 알려져 있다.[17] 반면에 본 연구에서처럼 해면질골 샘플의 초음파 입사면에 높은 밀도 및 음속을 갖는 피질골 판이 부착된 경우에는 정확한 감쇠계수를 구하기 위해 물/피질골 경계면에서 발생되는 투과손실이 보정되어야 한다. 그러므로 본 연구와 같이 식(2)로부터 얻어진 CTh.1.00, CTh.1.47, 및 CTh.2.00에 대한 감쇠계수는 임상에서 이용되는 초음파 골밀도 측정기의 경우와 마찬가지로 물/피질골 경계면에서 반사로 인해 발생되는 투과손실이 보정되지 않았으므로 엄밀히 말하면 겉보기 감쇠라고 할 수 있다. Fig. 4에서 볼 수 있듯이 서로 다른 두께를 갖는 피질골 판의 효과(피질골 경계면에서의 반사 및 피질골 내에서의 감쇠)로 인해 감쇠계수가 CTh.0 및 CTh.1.00의 경우에는 0.3-0.65 MHz, CTh.1.47 및 CTh.2.00의 경우에는 0.3-0.6 MHz와 같은 서로 다른 주파수 범위에서 선형적으로 증가하며, 또한 nBUA는 피질골 판의 두께에 대해 비선형적인 의존성을 나타내는 것을 알 수 있다. 본 연구와 유사하게 Xia 등도 18개의 사람 종골 샘플을 이용하여 해면질골 샘플의 양쪽 면에 존재하는 0.3 및 0.6 mm의 두께를 갖는 피질골 판이 nBUA의 측정에 큰 효과를 미치는 것을 보고하였다.[7]
IV. 결 론
본 연구에서는 생체 외 조건의 소 대퇴골에서 피질골이 해면질골의 SOS 및 nBUA와 같은 음향특성에 미치는 효과를 조사하기 위해 2개의 소 대퇴골을 이용하여 근위부로부터 12개의 해면질골 샘플 및 서로 다른 두께를 갖는 3개의 피질골 판을 제작하였다. 또한 해면질골 샘플에 피질골 판 부착 전후 측정된 음향특성과 해면질골 겉보기 골밀도 사이의 상관관계를 조사하였다. 해면질골 샘플의 초음파 입사면에 부착된 피질골 판의 두께가 증가함에 따라 SOS는 선형적으로 증가하는 반면에 nBUA는 피질골 판의 두께에 대해 비선형적인 의존성을 나타내는 것을 알 수 있었다. 또한 서로 다른 두께를 갖는 피질골 판이 부착되더라도 SOS 및 nBUA와 해면질골 겉보기 골밀도 사이의 높은 상관관계는 유지되는 것을 알 수 있었다. 이와 같은 결과는 생체 외 조건의 피질골이 제거되지 않은 대퇴골에서 측정된 음향특성이 해면질골의 골밀도를 예측하기에 충분한 지표라는 것을 의미한다. 그러므로 향후에는 후속연구로서 생체 내 조건의 사람을 대상으로 대퇴골의 음향특성을 측정하기 위한 초음파 측정시스템을 개발하고, 골다공증 진단지표로서 생체 내 조건의 대퇴골에서 측정된 음향특성의 타당성을 조사할 예정이다.