I. 서 론
베타 사이클로덱스트린(β-Cyclodextrin, β-CD)과 살리실산(salicylic acid), 알코올, 나프로젠, 이부프로펜 등에 대한 초음파 완화 연구는 많이 행하여지고 있다.[1-6] 사이클로덱스트린(Cyclodextrin,CD)는 몇 개의 글루코스단위로 구성되어 있는 올리고당이며 그 모양은 양쪽 면이 뚫린 양동이처럼 내부는 빈 공간이다. 내부는 소수성의 성질, 외부는 친수성의 성질을 가져 여러가지의 분자를 게스트로 하여 호스트와 게스트의 복합체를 형성한다.[7] Bae et al.[1-4]은 β-CD와 생체고분자에 대한 연구를 1 MHz 이하의 저주파수 영역에서 초음파 흡수 스펙트럼을 측정하여 호스트와 게스트의 복합체 형성과 붕괴반응에 대한 속도론적 연구를 행하였다.벤조산은 아스피린, 나프로젠, 이부프로펜 등과 같이 해열진통과 혈전예방제로 최근 아주 널리 사용되고 있는 비스테로이성 항염증제(Non-Steroidal Anti-Inflammatory Drugs, NSAIDs)의 일종이다. 그러나 NSAIDs은 위 점막에 국소 자극작용을 하는 특유의 성질을 가지기 때문에 위궤양 및 위출혈과 같은 부작용을 일으킨다. 이 부작용을 예방하기 위해 NSAIDs은 위 점막에 국소 자극작용을 하도록 특유의 성질을 가지게 하여, 위에서 오래 머물지 않고 소장으로 빨리 이동하도록 하여 많이 이용되고 있다.
β-CD를 호스트로, 여러가지의 생체고분자를 게스트로 한 복합체 형성과 붕괴반응에 의한 초음파 완화연구는 그 완화주파수가 수 MHz일 때 저 주파수영역의 극한 값을 정확히 측정하기가 곤란하여 종래의 초음파 흡수측정법으로는 속도론적 연구가 어렵다.[5,6] 본 연구는 CDs의 약물 방출 제어 능력을 평가하기 위하여 자연에서 가장 많이 존재하고, 2-매톡시 벤조산(2-methoxy benzoic acid)과 1:1의 복합체를 형성하는 글루코스가 7단위로 구성된 β-CD를 호스트 분자, 2-매톡시 벤조산(pH≈7.0)을 게스트 분자로 하여 복합체 형성과 붕괴반응의 속도론적 연구를 행하여, 같은 NSAIDs의 일종이고 벤조익산 유도체이며 벤조산에 수산기를 가지고 있는 살리실산과[6] 복합체 형성 속도상수, 붕괴상수, 평행상수, 체적변화를 비교하였다.
II. 실험방법
β-CD(시그마, c4767)와 2-매톡시 벤조산(시그마-알드리치, 169978)은 구입하여 그대로 사용하였다.또한 시료의 pH(pH≈7.0)은 NaOH를 사용하여 691 pH기( Ω Methohm, Swiss)로 측정하였다. 각 시료의 밀도는 DMA 5000M(anton Paar, Austria)을 사용하여 측정하였다. 모든 실험은 25 °C에서 행하였다. 초음파 흡수계수측정은 3종류의 측정법으로 0.2 MHz ~ 50 MHz영역에서 행하였다. 광 회절 초음파 공명법은 0.2 MHz ~ 1.7 MHz, 종래의 공명법은 2.4 MHz ~ 8.1 MHz, 광 편향법은 14 MHz ~ 50 MHz의 주파수 범위에서 초음파 흡수측정을 행하였다.
초음파 흡수계수측정은 3종류의 측정법으로 0.2 MHz ~ 50 MHz영역에서 행하였다. 광 회절 초음파 공명법은 0.2 MHz ~ 1.7 MHz, 종래의 공명법은 2.4 MHz ~ 8.1 MHz, 광 편향법은 14 MHz ~ 50 MHz의 주파수 범위에서 초음파 흡수측정을 행하였고, 각 측정법들은 5 % 이내로 초음파 흡수계수 측정이 가능하다. 초음파 공명법은 주파수 0.2 MHz ~ 10 MHz영역에서 액체의 흡수계수 측정에 아주 유효한 측정법이다. 공명법은 공명곡선의 반치 폭으로부터 흡수계수를 구한다. 종래의 공명법의 공명기는 수정진동자, 시료, 수정진동자로 구성되며, 한 개의 진동자는 음파를 발생하게 하고, 반대편의 수정진동자는 그 음파신호를 수신하게 하여 공명곡선을 구한다. 그러나 주파수 2 MHz 이하가 되면 음파의 회절의 영향이 나타나고 특히 1 MHz 이하에서는 흡수계수측정이 불가능하다. 10 MHz 이상에서는 흡수계수가 커지기 때문에 이웃하는 공명곡선들이 서로 겹치게 되어 또한 흡수계수측정이 불가능하여 광 편향법을 사용한다. 광 회절 초음파 공명법의 공명기는 수정진동자, 시료, 오목 반사판으로 구성되며, 오목 반사판은 회절의 영향을 줄이기 위하여 수정진동자 대신에 사용한다. 따라서 종래의 공명법으로 초음파 흡수측정이 불가능한 1 MHz 이하에서도 흡수계수측정이 가능하다. 광 편향법은 길이를 변화시키면서 음파의 진폭변화를 측정하는 방법으로 10 MHz 이하에서는 경로에 따른 진폭변화가 거의 없기 때문에 10 MHz 이상에서 흡수계수를 측정하는 유효한 수단이다. 그러나 50 MHz 이상에서는 경로에 따른 진폭변화가 급격히 작아져 흡수측정이 불가능하다. 광 회절 초음파 공명법은 선행 연구 발표에 상세히 기술되어 있다.[8] 광 편향법에 대해 간략하게 기술한다.[9] 초음파(파장λ)의 파면에 평행하게 광을 입사시킬 때 광폭이 λ보다 크면 라만·나스 회절이 일어나고, 광폭이 λ보다 작을 때는 광 편향이 일어난다. 편향각(θ)은 음파의 전파거리L과 굴절률(n)의 공간미분에 비례한다. 초음파에 의해 물질의 밀도변화가 일어나기 때문에 굴절률은 공간적(x), 시간적(t)으로 변화하고 θ는 초음파의 진폭과 주파수에 비례한다. 따라서 편향각의 시간변화를 측정하면 초음파의 진폭(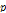 )의 변화에 비례하는 신호를 얻을 수 있다. 편향각(θ)은 다음과 같이 근사적으로 주어진다.
)의 변화에 비례하는 신호를 얻을 수 있다. 편향각(θ)은 다음과 같이 근사적으로 주어진다.
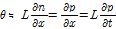
Fig. 1은 실험장치의 개략도이다. 광원으로는 출력 5 mW의 He-Ne 레이저를 사용했다. 광 편향법은 레이저 빔의 직경을 λ보다 충분히 작게 할 필요가 있다. 본 실험에서는 λ가 40 μm ~ 1.5 mm가 되기 때문에 빔의 직경을 수십 μm로 했다. 이를 위해 레이저 빔을 빔 익스팬더로 직경 10 μm로 넓혔다. 직경이 큰 빔의 회절은 작게 하기 때문에 폭이 좁은 빔을 만들 수 있다. 폭이 넓은 레이저 광은 초점거리 100 mm의 렌즈로 cell의 중심에 집속되도록 조절했다. 초음파셀을 통과한 레이저 빔은 다시 초점거리 100 mm의 렌즈로 집속시켜 포토다이오드에 입사시켰다. 검출된 신호는 증폭기를 통해 오실로스코프로 관측된다. 펠서에서 발진된 –250 V의 전기적 신호 DC펄스를 셀의 좌측에 있는 수정진동자에 가해 셀내에 초음파 펄스를 여기시킨다. DC펄스로 수정진동자를 여기하면 기본 주파수의 홀수배의 고조파를 포함하는 초음파가 시료에 여기되기 때문에 광대역의 주파수를 한꺼번에 관측할 수 있다. 사용된 X-커트 수정진동자의 기본주파수는 3 MHz이고 직경이 20 mm이다. 초음파 펄스의 전파거리를 변화시키면서 진폭을 관측하면 펄스에 포함된 14 MHz ~ 50 MHz의 고조파성분의 흡수계수를 구할 수가 있다. 초음파셀은 회전테이블 위에 놓여 있는 X-스테이지 위에 고정하였다. 회전테이블과 X-스테이지로 레이저 광과 음원과의 거리와 레이저 광의 입사각을 정밀히 조절했다. 이 실험장치의 흡수계수측정의 정확도는 물, 사이클로핵산, 벤젠의 문헌치와 비교해서 약 5 % 이내에서 일치하였다. 음속은 펄스 에코 오버랩법으로 측정하였다.
III. 결 과
Fig. 2는 2-매톡시 벤조산 (5 mM)과 β-CD(8.7 mM)의 수용액에 대한 초음파 흡수계수(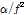 )를 주파수함수(
)를 주파수함수(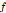 )로 나타내고 있다. 2-매톡시 벤조산에 대해서는 어떠한 완화현상도 관측되지 않았지만, 2-매톡시 벤조산과 β-CD수용액에 대해서는 완화현상이 관측됨을 알 수 있다. 한편 β-CD수용액의 초음파 완화현상은 13 mM 이상의 농도에서 관측되지만 그 이하의 농도에서는 관측되지 않는다.[10] 따라서 본 연구에서는 호스트인 β-CD의 농도를 일정(8.7 mM)하게 하고 게스트의 농도를 변화시키면서 초음파 흡수계수측정을 행하였다. Fig. 3은 2-매톡시 벤조산 수용액에 β-CD가 존재할 때의 대표적인 초음파 흡수스펙트럼을 보이고 있다. 관측된 완화현상의 스펙트럼을 해석하기 위하여 Debye형 단일완화식을 적용했다.[1,2,11]
)로 나타내고 있다. 2-매톡시 벤조산에 대해서는 어떠한 완화현상도 관측되지 않았지만, 2-매톡시 벤조산과 β-CD수용액에 대해서는 완화현상이 관측됨을 알 수 있다. 한편 β-CD수용액의 초음파 완화현상은 13 mM 이상의 농도에서 관측되지만 그 이하의 농도에서는 관측되지 않는다.[10] 따라서 본 연구에서는 호스트인 β-CD의 농도를 일정(8.7 mM)하게 하고 게스트의 농도를 변화시키면서 초음파 흡수계수측정을 행하였다. Fig. 3은 2-매톡시 벤조산 수용액에 β-CD가 존재할 때의 대표적인 초음파 흡수스펙트럼을 보이고 있다. 관측된 완화현상의 스펙트럼을 해석하기 위하여 Debye형 단일완화식을 적용했다.[1,2,11]
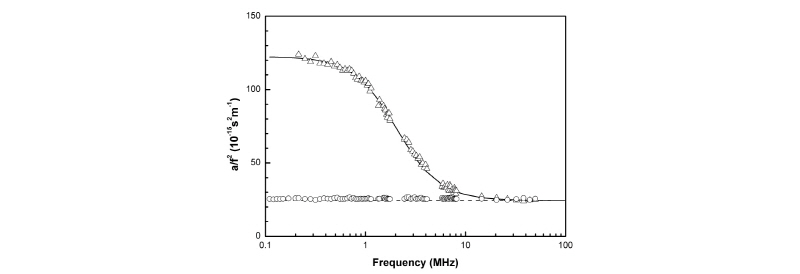
Fig. 2.
Ultrasonic absorption 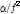 vs. frequency in aqueous solution of 2-methoxy benzoic acid at 25 °C in presence and absence of 8.7 mM β-CD:(○) 5mM 2-methoxy benzoic acid only, (△) 5 mM 2-methoxy benzoic acid+8.7 mM β-CD. The soild line represents the single relaxation curve. The dotted line represents the high-frequency limiting value
vs. frequency in aqueous solution of 2-methoxy benzoic acid at 25 °C in presence and absence of 8.7 mM β-CD:(○) 5mM 2-methoxy benzoic acid only, (△) 5 mM 2-methoxy benzoic acid+8.7 mM β-CD. The soild line represents the single relaxation curve. The dotted line represents the high-frequency limiting value 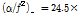
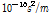 .
.
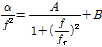 , (1)
, (1)
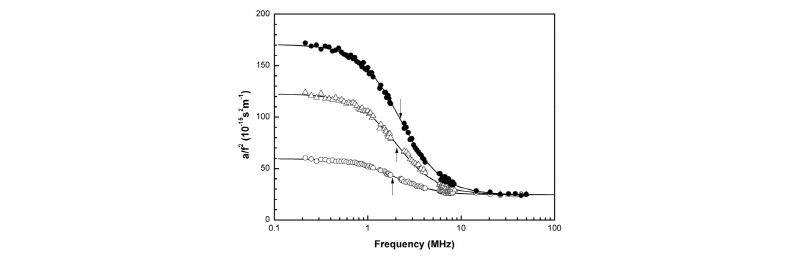
Fig. 3.
Representative ultrasonic absorption spectra in aqueous of 2-methoxy benzoic acid in the presence of 8.7 mMβ-CD at pH 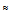 7.0 and 25 °C: (○) 1 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD; (△) 5 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD; (●) 10 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD. The solid lines represent the values calculated from equation (1). The arrows indicate the location of the relaxation frequency.
7.0 and 25 °C: (○) 1 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD; (△) 5 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD; (●) 10 mM methoxy benzoic acid + 8.7 8.7 mMβ-CD. The solid lines represent the values calculated from equation (1). The arrows indicate the location of the relaxation frequency.
여기서 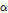 는 흡수계수,
는 흡수계수, 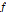 는 주파수이다.
는 주파수이다. 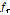 은 완화주파수,
은 완화주파수, 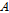 는 완화에 의한 흡수,
는 완화에 의한 흡수, 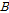 는 고전흡수이다. 흡수값
는 고전흡수이다. 흡수값 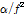 은 저주파수 영역에서는 주파수의 증가와 함께 증가하다가 일정하게 됨을 알 수 있다. 고주파수영역에서는
은 저주파수 영역에서는 주파수의 증가와 함께 증가하다가 일정하게 됨을 알 수 있다. 고주파수영역에서는 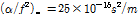 의 극한값에 접근함을 알 수 있다. 이 값은 25 °C의 물의 흡수값(
의 극한값에 접근함을 알 수 있다. 이 값은 25 °C의 물의 흡수값(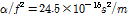 )과 거의 같고, 10 MHz 이상의 주파수영역에서는 어떠한 완화현상도 존재하지 않음을 알 수 있다. 실선은 Eq. (1)의
)과 거의 같고, 10 MHz 이상의 주파수영역에서는 어떠한 완화현상도 존재하지 않음을 알 수 있다. 실선은 Eq. (1)의 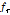 ,
, 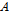 ,
,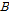 를 파라메타로 하여 실험치에 가장 일치하게 피팅한 것으로 이 피팅으로 부터
를 파라메타로 하여 실험치에 가장 일치하게 피팅한 것으로 이 피팅으로 부터 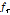 ,
, 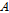 ,
,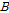 가 결정되고 이들 값은 Table 1 음속(
가 결정되고 이들 값은 Table 1 음속(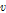 )과 밀도(
)과 밀도(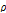 )와 함께 나타내었다. 그림에서 보는 바와 같이 실험치와 이론치(실선)가 잘 일치하고 있음을 알 수 있다. 화살표는 각 농도의 완화시간을 나타낸다. 초음파 완화현상은 β-CD와 2-매톡시 벤조산의 두 용질이 존재할 때 관측되기 때문에 다음의 평형반응의 혼란상태가 초음파 완화의 원인이라고 생각된다.[1,2,11]
)와 함께 나타내었다. 그림에서 보는 바와 같이 실험치와 이론치(실선)가 잘 일치하고 있음을 알 수 있다. 화살표는 각 농도의 완화시간을 나타낸다. 초음파 완화현상은 β-CD와 2-매톡시 벤조산의 두 용질이 존재할 때 관측되기 때문에 다음의 평형반응의 혼란상태가 초음파 완화의 원인이라고 생각된다.[1,2,11]
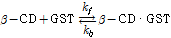 , (2)
, (2)
Table. 1. Ultrasonic and thermodynamic parameters for aqueous solutions of 2-methoxy benzoic acid (pH≈7.0) and β-CD (8.7 mM) at 25 °C. 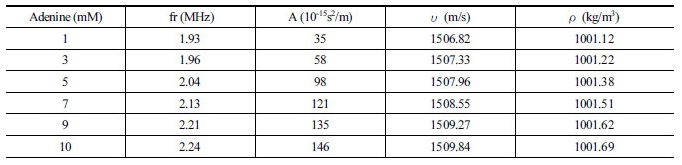 |
여기서 β-CD는 호스트이고 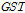 는 게스트 분자, β-CD ․ GST는 호스트와 게스트 분자에 의해 형성된 복합체이다.
는 게스트 분자, β-CD ․ GST는 호스트와 게스트 분자에 의해 형성된 복합체이다. 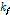 와
와 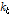 는 각각 복합체 형성과 붕괴 속도상수이다. 초음파 완화법으로 화학평행에 의한 속도상수와 체적변화를 해석하기 위해서는 중요한 두 개의 양이 만족스럽게 해석되어야 한다. 하나는 완화시간(
는 각각 복합체 형성과 붕괴 속도상수이다. 초음파 완화법으로 화학평행에 의한 속도상수와 체적변화를 해석하기 위해서는 중요한 두 개의 양이 만족스럽게 해석되어야 한다. 하나는 완화시간(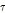 )이고, 또 하나는 완화진폭(
)이고, 또 하나는 완화진폭(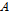 )이다. 완화시간과 반응물의 농도와의 관계식은 다음과 같다.[1,2,11]
)이다. 완화시간과 반응물의 농도와의 관계식은 다음과 같다.[1,2,11]
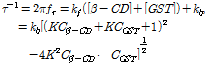 (3)
(3)
여기서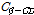 와
와 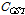 는 각각 β-CD와 GST의 초기농도이고, 평형상수
는 각각 β-CD와 GST의 초기농도이고, 평형상수 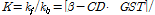
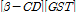 으로 정의된다. Table 1에서 보는 바와 같이
으로 정의된다. Table 1에서 보는 바와 같이 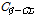 가 일정할 때
가 일정할 때 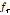 과
과 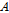 는
는 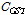 의 증가와 함께 증가함을 알 수 있다.
의 증가와 함께 증가함을 알 수 있다. 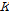 와
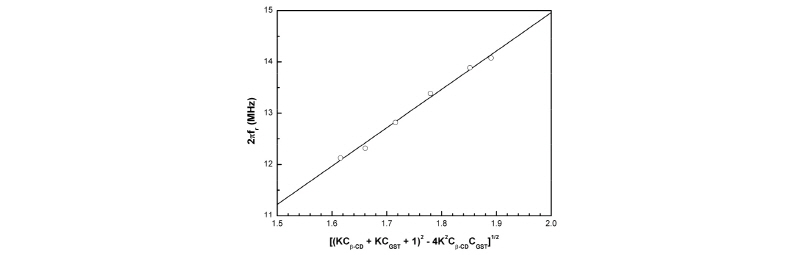
와 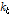 는 Eq. (3)에 의해 결정되어진다(Table 2). Fig. 4은 Eq. (3)에서 결정된
는 Eq. (3)에 의해 결정되어진다(Table 2). Fig. 4은 Eq. (3)에서 결정된 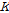 를 사용하여
를 사용하여 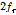 대
대 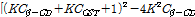
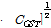 의 프로트이다. Fig. 4의 실선은
의 프로트이다. Fig. 4의 실선은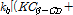
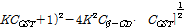 의 계산값이다. Fig. 4에서 이론치와 실험치가 잘 일치함을 알 수 있다.
의 계산값이다. Fig. 4에서 이론치와 실험치가 잘 일치함을 알 수 있다. 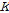 와
와 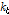 의 값들은 비스테로이드성 항염증제의 일종인 살리실산 (pH≈7.0)의 값들과 Table 2에 비교하였다. 복합체 형성속도상수
의 값들은 비스테로이드성 항염증제의 일종인 살리실산 (pH≈7.0)의 값들과 Table 2에 비교하였다. 복합체 형성속도상수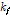 는
는 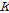 의 정의로부터 구해지고, 또한 Table 2에 나타내었다.
의 정의로부터 구해지고, 또한 Table 2에 나타내었다.
Table. 2. Rate and thermodynamic constants for Interaction between β-CD and 2-methoxy benzoic acid at 25 °C. 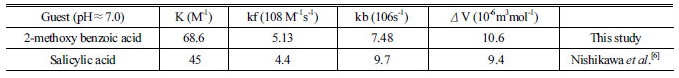 |
파장당 최대흡수치(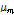 )는 초음파 완화와 관계되는 또 다른 중요한 양이다. 이것은 반응에 의한 표준체적변화(
)는 초음파 완화와 관계되는 또 다른 중요한 양이다. 이것은 반응에 의한 표준체적변화(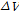 )와 관계되고, 다음과 같이 주어진다.[1,2,11]
)와 관계되고, 다음과 같이 주어진다.[1,2,11]
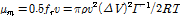 , (4)
, (4)
여기서 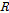 는 기체상수,
는 기체상수, 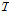 는 절대온도,
는 절대온도, 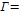
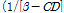
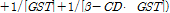 ,
, 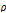 는 밀도,
는 밀도, 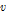 는 음속이다. 반응물질들의 평형농도는
는 음속이다. 반응물질들의 평형농도는 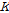 값, 그리고 2-매톡시 벤조산과
값, 그리고 2-매톡시 벤조산과 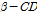 의 초기농도로부터 구할 수가 있다. 일반적으로 Eq. (4)의
의 초기농도로부터 구할 수가 있다. 일반적으로 Eq. (4)의 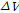 항을
항을 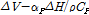 로 나타낸다. 여기서
로 나타낸다. 여기서 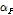 는 수용액의 열팽창계수,
는 수용액의 열팽창계수, 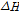 는 반응에 의한 표준엔탈피변화,
는 반응에 의한 표준엔탈피변화, 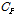 는 등압비열이다. 그러나 수용액에 대한 실험에서 열팽창계수가 아주 작기 때문에
는 등압비열이다. 그러나 수용액에 대한 실험에서 열팽창계수가 아주 작기 때문에 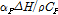 항은 무시한다. Fig. 5은
항은 무시한다. Fig. 5은 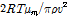 대
대 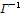 을 프로트한 것을 나타내고 있다. 2-매톡시 벤조익산의
을 프로트한 것을 나타내고 있다. 2-매톡시 벤조익산의 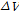 는 직선의 기울기로부터 구해지고, 그 값을 Table 2에 나타내었다.
는 직선의 기울기로부터 구해지고, 그 값을 Table 2에 나타내었다.
IV. 논 의
살리실산, AMP(Adenosine 5’-MonoPhosphate), c-AMP(Adenosine 3’, 5’-cyclic MonoPhosphate), 펜탄산, 아민산, 알코올을 게스트로, α-CD, β-CD를 호스트로 선택하여 행한 지금까지의 많은 연구에서 복합체형성 속도상수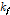 는 호스트, 게스트의 구조에 의존하지 않고, 거의 같은 확산속도정수의 값을 가지는 것을 알 수 있다.[1-6,11-13] 두 개의 분자들의 확산 반응속도는 Smoluchowski 식으로 설명할 수 있다.[11]
는 호스트, 게스트의 구조에 의존하지 않고, 거의 같은 확산속도정수의 값을 가지는 것을 알 수 있다.[1-6,11-13] 두 개의 분자들의 확산 반응속도는 Smoluchowski 식으로 설명할 수 있다.[11]
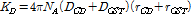 , (5)
, (5)
여기서 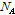 는 아보가드로 수,
는 아보가드로 수, 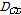 ,
, 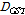 는 서로 반응하는 물질의 확산계수,
는 서로 반응하는 물질의 확산계수, 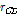 ,
, 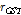 은 각각 호스트와 게스트의 분자의 반경이다. 많은 종류의 물질에 대해 확산 반응속도를 Eq. (5)로부터 계산하면
은 각각 호스트와 게스트의 분자의 반경이다. 많은 종류의 물질에 대해 확산 반응속도를 Eq. (5)로부터 계산하면 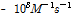 의 값이 얻어진다.[11-13] Table 2에서 우리들이 측정한
의 값이 얻어진다.[11-13] Table 2에서 우리들이 측정한 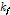 값은 확산속도와 거의 일치함을 알 수 있다. 따라서 게스트 분자인 2-매톡시 벤조산이 호스트 분자인 β-CD의 빈 공간으로 들어가는 복합체 형성 속도상수
값은 확산속도와 거의 일치함을 알 수 있다. 따라서 게스트 분자인 2-매톡시 벤조산이 호스트 분자인 β-CD의 빈 공간으로 들어가는 복합체 형성 속도상수 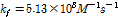 는 확산속도임을 알 수 있다.
는 확산속도임을 알 수 있다.
한편, 복합체 붕괴 속도상수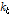 는 Table 2에서 알 수 있듯이 게스트 분자의 구조에 의존한다. 이전의 많은 연구에서
는 Table 2에서 알 수 있듯이 게스트 분자의 구조에 의존한다. 이전의 많은 연구에서 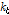 값은 게스트 분자의 소수성이 증가할수록 감소함을 알았다.[1-6,11-13] 복합체의 안정성은 게스트 분자가 호스트 내부에서 떨어지는 붕괴 속도상수에 의해 결정된다. 게스트 분자의 소수성이 강하면 강할수록 β-CD내부에서 소수성 결합이 강하여 복합체 형성이 안정되므로
값은 게스트 분자의 소수성이 증가할수록 감소함을 알았다.[1-6,11-13] 복합체의 안정성은 게스트 분자가 호스트 내부에서 떨어지는 붕괴 속도상수에 의해 결정된다. 게스트 분자의 소수성이 강하면 강할수록 β-CD내부에서 소수성 결합이 강하여 복합체 형성이 안정되므로 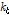 값은 작아진다. 2-매톡시 벤조산의
값은 작아진다. 2-매톡시 벤조산의 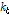 값은 살리실산에 비해 Table 2에서 보는 바와 같이 1.3배 작다. 이것은 2-매톡시 벤조산이 살리실산보다 소수성이 강하여 β-CD와 안정한 복합체를 형성한다는 것을 의미한다. 따라서 β-CD-NSAIDs계가 약물수송에 응용된다면 산성의 환경인 위내에서 β-CD는 2-매톡시 벤조산을 살리실산보다 늦게 방출되기 때문에 위장에서 2-매톡시 벤조산이 보다 오래 동안 머물 수 있다는 것을 알 수 있다. Table 2에서 2-매톡시 벤조산의
값은 살리실산에 비해 Table 2에서 보는 바와 같이 1.3배 작다. 이것은 2-매톡시 벤조산이 살리실산보다 소수성이 강하여 β-CD와 안정한 복합체를 형성한다는 것을 의미한다. 따라서 β-CD-NSAIDs계가 약물수송에 응용된다면 산성의 환경인 위내에서 β-CD는 2-매톡시 벤조산을 살리실산보다 늦게 방출되기 때문에 위장에서 2-매톡시 벤조산이 보다 오래 동안 머물 수 있다는 것을 알 수 있다. Table 2에서 2-매톡시 벤조산의 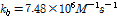 는 S. Nishikawa et al가 살리실산(pH≈7.0)에 대해 초음파 흡수측정으로부터 구한
는 S. Nishikawa et al가 살리실산(pH≈7.0)에 대해 초음파 흡수측정으로부터 구한 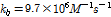 보다 약 1.3배,
보다 약 1.3배, 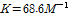 값은 1.5배 정도 작았다. 2-매톡시 벤조익산은 벡조산에 메칠기를, 살리실산은 벤조산에 수산기를 가지고 있다. 메칠기는 수산기 보다 더 소수성이기 때문에 β-CD내부로 깊게 들어갈 수 있다. 따라서 위내에서 β-CD는 2-매톡시 벤조산을 살리실산보다 늦게 방출한다.
값은 1.5배 정도 작았다. 2-매톡시 벤조익산은 벡조산에 메칠기를, 살리실산은 벤조산에 수산기를 가지고 있다. 메칠기는 수산기 보다 더 소수성이기 때문에 β-CD내부로 깊게 들어갈 수 있다. 따라서 위내에서 β-CD는 2-매톡시 벤조산을 살리실산보다 늦게 방출한다.
다음으로 복합체 형성과 붕괴반응에 의한 체적변화(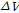 )를 고찰한다. 수용액상태에서 β-CD 내부에는 7-8 개의 물 분자가 존재한다.[7] 게스트 분자가 β-CD내부로 들어가면 몇 개의 물 분자가 밖으로 나온다.
)를 고찰한다. 수용액상태에서 β-CD 내부에는 7-8 개의 물 분자가 존재한다.[7] 게스트 분자가 β-CD내부로 들어가면 몇 개의 물 분자가 밖으로 나온다. 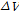 값의 기여는
값의 기여는 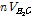 이다. 여기서
이다. 여기서  는 β-CD에서 밖으로 나오는 물 분자의 수이다. 체적변화에 대한 음의 기여(
는 β-CD에서 밖으로 나오는 물 분자의 수이다. 체적변화에 대한 음의 기여(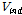 )는 게스트 분자가 β-CD내부로 들어 갔을 때이다. 결국 체적변화는 간단하게
)는 게스트 분자가 β-CD내부로 들어 갔을 때이다. 결국 체적변화는 간단하게 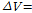
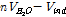 로 표현할 수 있다. S. Nishikawa et al은
로 표현할 수 있다. S. Nishikawa et al은 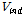 가 벤젠의 몰부피이라 생각하고
가 벤젠의 몰부피이라 생각하고 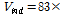
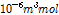 의 값을 가지고 보고 했다.[6]
의 값을 가지고 보고 했다.[6] 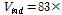
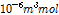 의 값은 β-CD내로 벤젠이 완전히 들어 가면 4.6개의 물분자가 방출됨을 알 수 있다. β-CD와 많은 게스트 분자들과의 복합체 형성과정의 연구에서
의 값은 β-CD내로 벤젠이 완전히 들어 가면 4.6개의 물분자가 방출됨을 알 수 있다. β-CD와 많은 게스트 분자들과의 복합체 형성과정의 연구에서 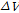 의 값은 항상 양이다. 따라서 β-CD와 살리실산(pH≈7.0)의 복합체 결합과정에서
의 값은 항상 양이다. 따라서 β-CD와 살리실산(pH≈7.0)의 복합체 결합과정에서 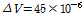
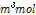 이므로 β-CD로 부터 약7.1개의 물 분자가 나온다고 계산할 수 있다. 2-매톡시 벤조산과 β-CD가 복합체를 형성할 때의
이므로 β-CD로 부터 약7.1개의 물 분자가 나온다고 계산할 수 있다. 2-매톡시 벤조산과 β-CD가 복합체를 형성할 때의 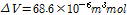 는 살리실산과 β-CD가 복합체를 형성할 때의
는 살리실산과 β-CD가 복합체를 형성할 때의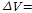
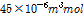 보다 큰 값을 가진다. 이것은 2-매톡시 벤조산이 살리실산보다 β-CD내부로 보다 깊숙히 들어가 β-CD내의 물분자 보다 더 많이 밖으로 방출된다는 의미이다. 2-매톡시 벤조산의 경우 약 8.4개의 물분자가 β-CD내에서 밖으로 나간다는 것을 알 수 있다.
보다 큰 값을 가진다. 이것은 2-매톡시 벤조산이 살리실산보다 β-CD내부로 보다 깊숙히 들어가 β-CD내의 물분자 보다 더 많이 밖으로 방출된다는 의미이다. 2-매톡시 벤조산의 경우 약 8.4개의 물분자가 β-CD내에서 밖으로 나간다는 것을 알 수 있다.
V. 결 론
β-CD를 호스트 분자, 2-매톡시 벤조익산을 게스트 분자로 선택하여 초음파 완화법을 사용해서 복합체 형성과 붕괴반응의 속도론적 연구를 행하여 살리실산과 비교한 결과, (1) 복합체 형성반응 속도정수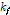 는 확산속도 정수 값을 가지고, 복합체 붕괴반응 속도정수
는 확산속도 정수 값을 가지고, 복합체 붕괴반응 속도정수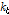 는 2-매톡시 벤조산이 살리실산보다 작은 값을 보였다. 이는 2-매톡시 벤조산이 살리실산 보다 소수성이 강하는 것을 알 수 있고, 또한 장내에서 2-매톡시 벤조산이 살리실산보다 늦게 흡수됨을 알 수 있다. (2) 복합체 형성과 붕괴반응에 의한 체적변화
는 2-매톡시 벤조산이 살리실산보다 작은 값을 보였다. 이는 2-매톡시 벤조산이 살리실산 보다 소수성이 강하는 것을 알 수 있고, 또한 장내에서 2-매톡시 벤조산이 살리실산보다 늦게 흡수됨을 알 수 있다. (2) 복합체 형성과 붕괴반응에 의한 체적변화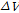 는 살리실산보다 큰 값을 보였다. 따라서 2-매톡시 벤조산과 β-CD가 복합체를 형성할 때 β-CD내에서 밖으로 나가는 물 분자수는 살리실산의 약 7.1개 보다 많은 약8.4개임을 알 수 있다. (3) β-CD - NSAIDs계의 약물수송에 대한 보다 많은 정보를 얻기 위해서는 여러종류의 NSAIDs계의 초음파 흡수측정을 행하여 복합체 붕괴반응 속도정수
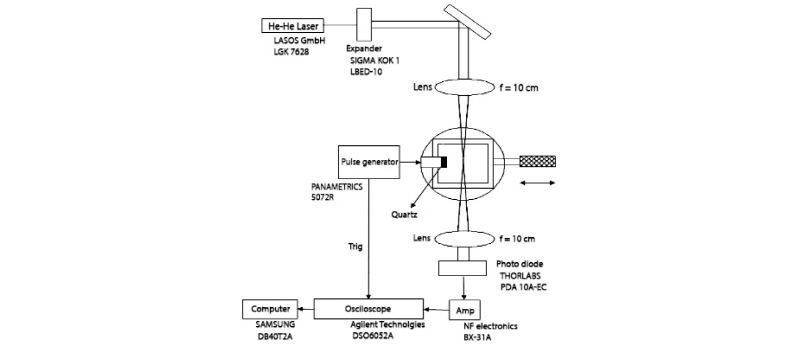
는 살리실산보다 큰 값을 보였다. 따라서 2-매톡시 벤조산과 β-CD가 복합체를 형성할 때 β-CD내에서 밖으로 나가는 물 분자수는 살리실산의 약 7.1개 보다 많은 약8.4개임을 알 수 있다. (3) β-CD - NSAIDs계의 약물수송에 대한 보다 많은 정보를 얻기 위해서는 여러종류의 NSAIDs계의 초음파 흡수측정을 행하여 복합체 붕괴반응 속도정수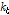 의 정량화가 필요하다.
의 정량화가 필요하다.



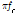 vs
vs 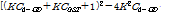
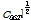 for aqueous solution of 2-methoxy benzoic acid in the presence of 8.7 mM β-CD at 25 °C.
for aqueous solution of 2-methoxy benzoic acid in the presence of 8.7 mM β-CD at 25 °C.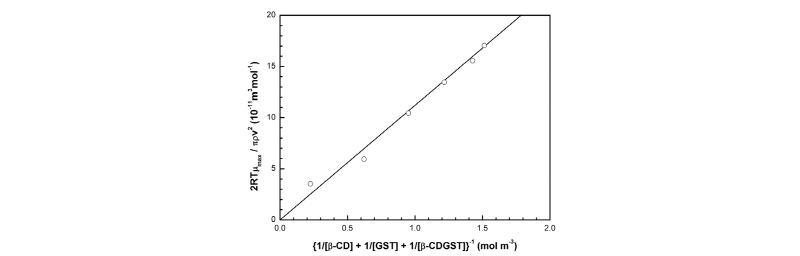
 vs
vs 
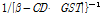 for aqueous solutions of 2-methoxy benzoic acid in the presence of 8.7 mM β-CD at 25 °C.
for aqueous solutions of 2-methoxy benzoic acid in the presence of 8.7 mM β-CD at 25 °C.
