I. 서 론
II. 연구방법
2.1 Echogenic liposome 제조
2.2 에너지여과 투과전자현미경(EF-TEM)을 이용한 구조분석
2.3 크기 분포 측정
2.4 세포 배양
2.5 Sonoporation 실험 및 WST-1 assay를 이용한 세포 생존율 측정
III. 결 과
3.1 EF-TEM
3.2 크기 분포
3.3 세포 생존율
IV. 고찰 및 결론
I. 서 론
혈관 내에서 자유로이 이동 가능한 공학적으로 가공된 미소기포는 이미 초음파 조영제로서 초음파 영상 내 반사 대비를 높여 진단에 도움을 주고 있다.[1,2] 또한, 이러한 미소기포의 좀 더 파괴적인 공동화 효과를 약물전달에 적용하여 spatially targeting 가능한 약물전달 매개체로 연구되고 있다.[3,4,5,6] 일반적으로 공학 기술이 접목된 미소기포의 내부는 perfluorocarbon gas와 같은 안정성이 높은 core와 그를 둘러싼 shell로 구성되어 있다. 이 때 shell로는 생체적합 재료인 인지질 혹은 알부민 등이 널리 사용되고 있다.[7]
cavitation은 통상 stable cavitation과 inertia cavitation으로 구분된다. stable cavitation은 음향압력 진폭이 낮아 기포가 수축과 팽창을 반복한 경우이다. 이 현상이 경계면에서 발생 시 microstreaming이 일어나 전단응력이 유도되며 세포막과 같은 생체 장벽에 약물 투과 효율을 높여 줄 수 있다.[8,9] 반면, inertia cavitation은 높은 진폭을 갖는 초음파에 노출되었을 때, 기포가 빠르게 팽창한 후 붕괴하는 현상을 의미한다. 이러한 기포의 붕괴는 경계면 부근에서 비대칭적으로 일어나며, 그 결과 나타나는 microjet은 경계면의 장벽 기능을 일시적으로 떨어뜨려 약물 투과 효율을 향상시킨다.[10,11] 이렇듯 cavitation은 초음파 기반 약물전달 기술인 sonoporation의 주요 매커니즘이고, 미소기포는 sonoporation에서 핵심적인 약물전달체이다.[12,13,14]
앞선 선행 연구에서 인지질을 shell로 하고 perfluorobutane을 core로 하는 미소기포 제작방식에 대하여 보고하였다.[15,16] 또한, 제작된 기포의 상당수가 내부에 유체를 함께 포함할 수 있는 구조임을 검증하였다.[15] 이러한 구조의 미소기포는 초음파에도 반응할 수 있고 한편으로는 약물 탑재가 가능할 수 있어 echogenic liposome이라 한다. 본 연구에서는 개발된 echogenic liposome의 구조에 실제 약물이 탑재되었을 때 약물전달 효과 개선에 미치는 영향을 실험적으로 입증하고자 한다.
Doxorubicin(Dox)은 유방암과 악성 림프종과 같은 질병을 치료하는 데 가장 자주 사용되는 항암제 중 하나이다. Dox는 인체 유방암 세포주 MDA-MB-231에서 세포사멸을 활성화하는 caspase-3과 caspase-8의 유전자 발현을 감소시키고, 세포사멸 매커니즘의 핵심 조절자인 B-cell lymphoma-2(Bcl-2) 단백질 발현을 감소시킴으로써, 세포사멸을 유도한다. 또한, 세포 성장을 억제하는 superoxide dismutase 2(SOD2)의 유전자와 단백질 발현을 증가시킨다.[17] 하지만, Dox는 종양 세포뿐만이 아니라 정상세포에도 영향을 끼치며, 심장 독성(cardiotoxicity)과 신독성(nephrotoxicity)을 야기한다는 부작용이 존재한다.[18] 이러한 문제를 해결하기 위해 약물을 echogenic liposome에 탑재하여 적은 양의 약물만 원하는 표적부위에 전달하는 방식이 이상적일 수 있다.[19] 따라서, echogenic liposome의 Dox 전달 효과를 MDA-MB-231 세포 대상으로 전임상 실험을 통하여 입증하였다.
II. 연구방법
2.1 Echogenic liposome 제조
증류수 50 ml와 프로필렌 글리콜(Sigma-Aldrich, St Louis, Mo, USA) 52.5 ml, 글리세롤(Sigma-Aldrich, St Louis, Mo, USA) 2.5 ml를 섞는다. 이 혼합물에 1,2- dipalmitoyl-sn-glycero-3-phosphocholine(DPPC, Avanti Polar Lipids Inc., USA) 0.105 g과 음이온성 지질인 1,2- dihexadecanoyl-sn-glycero-3-phosphate(DPPA, Avanti Polar Lipids Inc., USA) 0.0105 g, 콜레스테롤(Avanti Polar Lipids Inc., USA) 0.0315 g을 섞은 후, 핫플레이트(HSD180, MTOPS, Korea)로 60 °C에서 30 min 가열하여 녹인다.
완전히 용해된 것이 확인되면, 혼합물을 2 ml 바이알에 2000 µl 씩 분주한 후, -15 °C에서 1 h 이상 냉각시킨다. 그다음 혼합물이 들어있는 바이알에 액화상태인 perfluorobutane(PFB)을 20 µl를 섞은 후, 밀봉하여 준비한다. 준비된 용액을 vialmixer(Lantheus Medical Imaging Inc., North Billerica, MA, USA)를 사용하여 45 s 동안 흔들어 제작하였다. 제작 후, 바이알의 온도는 최대 40 °C에 달하므로 만들어진 미소기포 용액은 1 °C에서 1 h 동안 냉각하였다.
2.2 에너지여과 투과전자현미경(EF-TEM)을 이용한 구조분석
제작된 echogenic liposome의 구조는 에너지여과 투과전자현미경(LIBRA 120, Carl Zeiss Inc., Oberkochen, Germany)을 사용하여 분석하였다. 미소기포 용액 10 µl를 200 mesh TEM grid(Ted Pella Inc., Redding, CA, USA)에 1 min 동안 고정한 후, 여과지로 남은 잔여물을 닦았다. 그리고 Uranyl Acetate(UA)로 10 s 동안 염색을 진행한 후, 남은 UA는 여과지로 흡수한 후, EF-TEM을 사용하여 이미지를 얻었다.
2.3 크기 분포 측정
미소기포의 크기는 Dynamic Light Scattering(DLS)을 이용한 입자크기 분석기(Zetasizer Nano ZS90, Malvern Instruments Ltd., U.K.)를 이용하여 측정하였다. 각 미소기포들은 측정 전, 증류수와 1:4로 희석하여 측정되었고, 정확한 측정을 위해 하나의 표본당 3번 측정을 진행하였으며, 각 측정당 15회 반복 측정하여 평균을 얻었다.
2.4 세포 배양
실험에 사용된 인체 유방암 세포 MDA-MB-231은 한국 세포주은행(Korea Cell Line Back, Seoul, Korea)에서 구매하여 사용하였다. 세포는 10 % Fetal Bovine Serum(FBS), 100 U/ml penicillin, 100 µg/ml streptomycin이 포함된 RPMI1640(Welgene, Korea) 배지에서 5 % CO2, 37 °C 조건으로 세포배양기에서 배양되었다.
2.5 Sonoporation 실험 및 WST-1 assay를 이용한 세포 생존율 측정
배양된 MDA-MB-231 세포를 12 well plate에 각 well 당 1 × 105씩 seeding한 후, 세포가 각 well의 80 % ~ 90 %가 도달할 때까지 10 % FBS를 함유하는 배지에서 배양되었다. 배양된 세포는 4개의 그룹으로 나누었으며, 각 그룹은 24 h와 48 h 후로 나누어 세포 생존율을 측정하였다. 첫 번째 그룹은 비교군으로 아무 처리도 하지 않은 그룹이다. 두 번째 그룹은 1 µM의 doxorubicin을 넣은 그룹이고, 세 번째 그룹은 1 µM의 doxorubicin과 별도로 제작된 echogenic liposome을 섞은 후, 초음파를 조사한 그룹으로, Park et al.[20]에 따라 calibration된 초음파 시스템을 1 MHz 주파수로 1 MPa 음압, 0.3 W/cm2 강도, 1 % duty rate로 10 s 동안 초음파를 조사하였다. 이 때 echogneic liposome을 1 % FBS가 포함된 RPMI1640 배지에 1000:1의 비율로 섞어 넣었다. 마지막 그룹은 1 mM의 doxorubicin을 포함한 미소기포를 배지에 1000:1 비율로 섞어 최종적으로 1 µM이 되도록 만든 후, 동일한 조건의 초음파를 조사한 그룹이다.
MDA-MB-231 세포의 세포 생존율은 EZ-cytox cell viability assay kit(Daeil Labservice, Seoul, Korea)를 사용하여 측정되었다. 24 h과 48 h 후에 WST-1 용액을 각 well에 1:10 비율로 첨가하고 plate를 세포배양기에서 30 min 동안 추가로 배양하였다. 세포생존율은 Microplate reader(Epoch, BioTek Instruments, Winooski, VT, USA)를 사용하여 450 nm 파장에서 측정되었다.
III. 결 과
3.1 EF-TEM
제작된 미소기포의 EF-TEM 이미지는 다음 그림과 같다(Fig. 1). 이전 보고에서와 같이 50 % 이상의 미소기포가 echogenic liposome의 구조를 형성함을 알 수 있다.[15] 중심에 밝게 나타나는 기체층 주변의 유체층이 shell 내부에 존재하며, 이 공간은 다른 기포와는 달리 표면이나 shell의 영역이 아닌 내부의 3차원 공간에 수용성 약물을 탑재할 수 있다.
3.2 크기 분포
PFB의 양에 따른 크기 분포에 관한 결과는 다음 그림과 같다(Table 1). 평균적인 크기는 약 1241 nm이며, 전체적으로 500 nm ~ 2 µm 분포를 나타낸다. 이러한 크기 분포는 실제 혈관 내에서 자유로이 이동할 수 있는 크기의 한계인 3 µm보다 작아 인체에 적용할 수 있다. 또한, shell의 영향으로 공진 주파수가 높아질 수는 있으나 일반적으로 의료 초음파에서 많이 사용되는 1 MHz ~ 10 MHz 영역에서 민감하게 반응할 수 있는 미소기포의 조건에 충족한다.[21,22] 따라서 sonoporation에 사용이 적합한 전달체 크기이다.
Table 1.
Size distribution of the microbubbles.
3.3 세포 생존율
세포 생존율은 각 그룹에 미소기포와 Dox, 초음파 조사 후, 24 h과 48 h 후에 WST-1 assay를 이용해 측정되었다(Fig. 2). Dox only 그룹의 24 h과 48 h 변화를 비교해 보면 92.9 %와 68.9 %로 시간에 따라 크게 변화함을 알 수 있다. 이는 1 µM 농도의 Dox 확산에 의한 세포의 괴사 결과는 일정 시간이 소요되기 때문이다. 반면 Dox + MB + US 그룹의 세포 생존율은 24 h 후 92.0 %와 48 h 후 64.5 %로 각각 관측되었다. 이는 sonoporation의 효과가 통계적 차이를 보일 정도에 이르기는 하나 급격히 향상되었다 주장하기는 어렵다. 이와는 대조적으로 Dox를 탑재한 echogenic liposome의 경우 세포 생존율이 24 h 후 70.5 %와 48 h 후 54.2 %로 다른 방법들에 비해 그 약물전달 효과가 크게 향상되었다. 이는 처음부터 개별 세포에 전달된 Dox의 양도 상대적으로 높으며, 더 많은 세포에 효과적으로 전달되었음을 의미한다. 따라서 제안된 echogenic liposome의 약물 전달체로의 활용 가능성이 크다고 볼 수 있다.
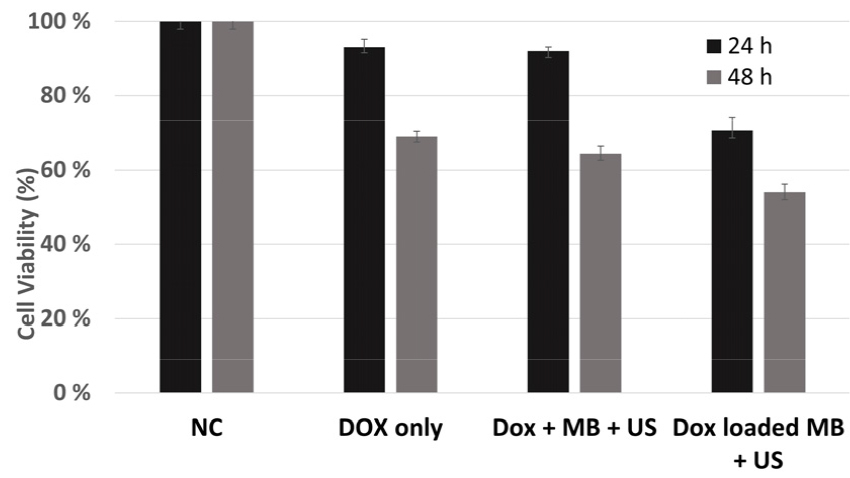
Fig. 2.
Cell viability test result. Untreated NC group, Dox only group with Dox 1 µM, Dox + MB + US group with Dox 1 µM and MB diluted 1000:1 mixed together, Dox loaded MB + US group with MB produced with Dox 1 mM diluted 1000:1. Cell viability was progressed through WST-1 assay and expressed as a percentage based on the NC group.
IV. 고찰 및 결론
실험에서 사용되는 echogenic liposome을 제작할 때 20 µl의 액화 상태의 perfluorobutane을 넣고 Vialmixer로 에너지를 전달하면 vial 내부의 압력도 크게 상승한다. 이는 끓는점이 약 – 2.5 °C인 perfluorobutane이 일부 기화되기 때문이다. 그러나 높아진 압력으로 끓는점이 약 – 2.5 °C인 perfluorobutane이 일부 기화되기 때문이다. 그러나 높아진 압력으로 끓는점이 상승하기에 모든 perfluorobutane이 기화하지는 못할 것이다. 이는 압력이 상승함에 따라 끓는점이 높아지기 때문이다. 실제 냉각까지 완료한 vial의 압력을 디지털 압력계(ADT681, Additel Corporation, USA)를 사용하여 측정한 결과 약 4.6 psi로 확인되었다. Clausius Clapeyron equation에 따르면 주어진 조건에서 perfluorobutane의 끓는점은 30 °C 이상으로 상승하리라 예측할 수 있다. 따라서 상당히 많은 양의 기화된 perfluorobutane은 냉각시간 동안 액화하였을 것이다. 이렇게 액화할 때 부피가 급격히 줄어듦에 따라 최초에 생성된 단순한 기포의 shell 내부로 외부 유체를 일부 끌어들일 것으로 예상할 수 있다. 결과적으로 일반적인 기포의 구조가 아닌 TEM에서 관측할 수 있는 echogenic liposome이 생성될 것으로 보인다. 다만, 현재는 이러한 변화 현상을 직접적이며 즉각적으로 관측하기 어려워 입증에는 추가적인 실험이 필요하다.
약물을 탑재한 형태의 미소기포는 다양한 방식으로 제안되고 연구되고 있다. 그 중 대표적인 것이 A. Kheirolomoom et al.[23]이 제안한 기포에 별도의 liposome들을 붙이는 형태이다. 이는 하나의 complex로 형태로 sonoporation에 적절한 구조이기는 하다. 다만, 기포자체가 구조적으로 안정성이 떨어지게 되어있다. 구 형태의 기포는 반경에 반비례하는 Laplace pressure가 작용하여 그 수명이 짧을 수밖에 없다.[24] 따라서 기포 생성 후 추가적인 단계를 거쳐야 하는 complex 구조체를 대량으로 생성하기 어렵다. 그에 비하여 제안된 방식의 echogenic liposome의 경우 충분한 수의 약물 전달체를 제공한다. 또한, Vialmixer로 활성화하지 않으면 1주일 이상 보관하여 사용도 가능하여 실용성에서도 상당한 장점이 있다.
본 실험에서 사용된 Dox의 용량은 참고한 논문에서 사용되는 용량에 약 1/5 수준이다.[24]이는 전달 효과를 비교하기 위한 기술적 방법으로 선택한 것이다. 따라서 실질적인 상황에서는 더욱 높은 농도의 Dox를 사용할 수 있어 암 치료에 효과적일 수 있을 것으로 예상한다.
본 연구에서는 단순한 기포가 아닌 약물 탑재가 가능한 echogenic liposome을 제안하였다. 그 구조적 특성을 TEM으로 확인하였으며, 약물전달 효과의 우수성을 세포실험을 통하여 입증하였다. 향후 sonoporation에 제안된 echogenic liposome이 더욱 안전하고 효과적으로 다양한 약물을 전달하여 암 등 다양한 질환에 활용될 수 있을 것으로 기대된다.





